
Q CELLS: Conoce al Gigante de la Energía Solar
Descubre Q CELLS, el líder mundial en paneles solares. Conoce su historia, la innovación alemana...
En el mundo que nos rodea, desde la sal que sazona nuestros alimentos hasta las gemas preciosas, existen estructuras cristalinas de una solidez y estabilidad asombrosas. ¿Alguna vez te has preguntado qué fuerza mantiene unidos a estos átomos de forma tan ordenada y tenaz? La respuesta reside en un concepto fundamental de la química: la energía reticular. Esta energía es la medida de la fuerza cohesiva en los compuestos iónicos, el pegamento invisible que dicta su dureza, su punto de fusión y su propio ser. Comprenderla es desvelar uno de los secretos mejor guardados sobre la estabilidad de la materia.
La energía reticular, también conocida como energía de red, puede definirse desde dos perspectivas complementarias, como las dos caras de una misma moneda. Ambas definiciones son correctas y describen el mismo fenómeno energético desde puntos de vista opuestos. La elección de una u otra depende del proceso que se esté describiendo, y es la clave para responder si su valor es positivo o negativo.

Esta es la definición más formal. La energía reticular es la energía que se necesita suministrar para separar completamente un mol de un compuesto iónico en estado sólido y convertirlo en sus iones constituyentes en estado gaseoso, infinitamente alejados unos de otros. Pensemos en un cristal de sal de mesa (NaCl). Para romper todas las atracciones entre los iones Na⁺ y Cl⁻ y dejarlos como un gas de iones individuales, debemos aplicar energía. Como el sistema absorbe energía del entorno para que ocurra esta separación, el proceso es endotérmico. Por convención, a los procesos endotérmicos se les asigna un valor de energía positivo. Por lo tanto, bajo esta definición, la energía reticular es siempre positiva.
NaCl(s) + Energía → Na⁺(g) + Cl⁻(g) (ΔH > 0)
Esta definición describe el proceso inverso. Aquí, la energía reticular es el cambio de energía que ocurre cuando un mol de un compuesto iónico sólido se forma a partir de sus iones en estado gaseoso. Imaginemos una nube de iones de sodio positivos (Na⁺) y iones de cloruro negativos (Cl⁻) flotando libremente. Cuando se atraen y se ordenan para formar la estructura estable de un cristal de sal, liberan una enorme cantidad de energía en forma de calor. Este proceso es altamente favorable y espontáneo. Como el sistema libera energía al entorno, el proceso es exotérmico, y por convención, se le asigna un valor de energía negativo. Bajo esta definición, a menudo llamada “entalpía reticular de formación”, el valor es siempre negativo.
Na⁺(g) + Cl⁻(g) → NaCl(s) + Energía (ΔH < 0)
En resumen, la magnitud de la energía es la misma en ambos casos; solo cambia el signo para indicar la dirección del proceso. Un valor absoluto alto siempre indica una red cristalina más fuerte y un compuesto más estable.
El valor de la energía reticular no es un simple dato académico; tiene implicaciones prácticas y predictivas muy importantes. Nos permite entender y predecir propiedades físicas clave de los compuestos iónicos.
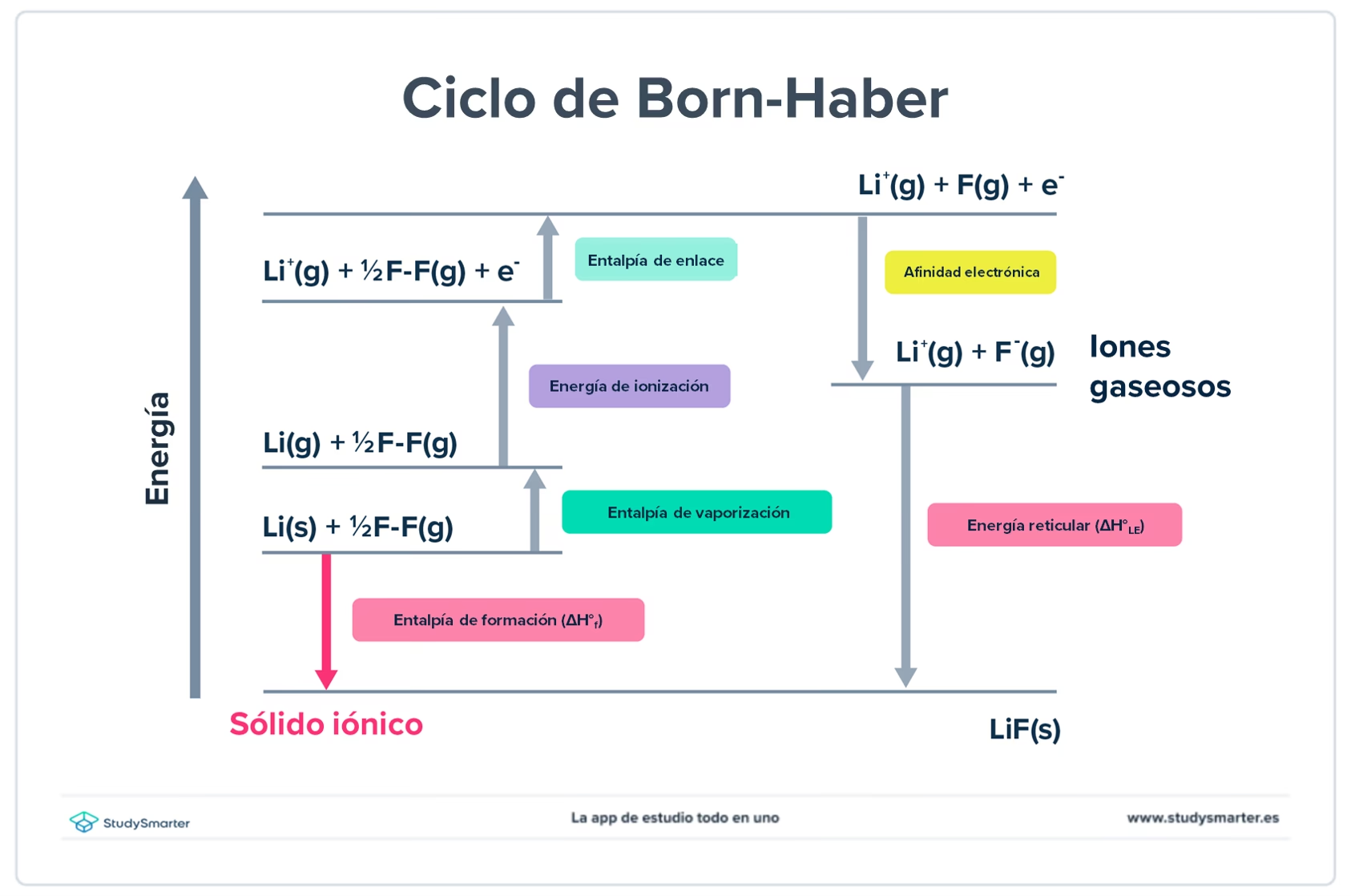
Un hecho fascinante sobre la energía reticular es que no se puede medir directamente en un laboratorio. No podemos simplemente tomar un puñado de iones gaseosos y medir el calor que liberan al formar un cristal. Para superar este obstáculo, los químicos Max Born y Fritz Haber desarrollaron un ingenioso método indirecto a principios del siglo XX: el ciclo de Born-Haber. Este ciclo es una aplicación brillante de la Ley de Hess, que establece que el cambio total de entalpía en una reacción química es el mismo, independientemente de los pasos intermedios que se tomen. El ciclo descompone la formación de un compuesto iónico en una serie de pasos hipotéticos cuyas energías sí pueden medirse experimentalmente:
Conociendo los valores energéticos de todos estos pasos, la energía reticular es la única incógnita que queda en el ciclo. Aplicando la Ley de Hess, podemos calcularla con gran precisión. Es la pieza que completa el rompecabezas energético.
¿Qué hace que un compuesto tenga una energía reticular mayor que otro? La respuesta se encuentra en la ley fundamental de la electrostática: la Ley de Coulomb. La fuerza de atracción entre dos cargas es directamente proporcional al producto de las cargas e inversamente proporcional a la distancia que las separa. Esto se traduce en dos factores principales:
Este es el factor más dominante. A mayor carga en los cationes y aniones, la atracción será mucho más fuerte. Por ejemplo, el óxido de magnesio (Mg²⁺O²⁻) tiene una energía reticular (-3795 kJ/mol) casi cinco veces mayor que la del fluoruro de litio (Li⁺F⁻) (-1030 kJ/mol), aunque sus iones tienen tamaños similares. La atracción entre cargas +2 y -2 es inmensamente superior a la de +1 y -1, lo que se refleja en una estabilidad mucho mayor.
A menor distancia entre los centros de los iones, mayor será la fuerza de atracción. Esto significa que los compuestos formados por iones más pequeños tendrán, en general, energías reticulares mayores. Por ejemplo, si comparamos los haluros de sodio (NaF, NaCl, NaBr), el NaF tiene la mayor energía reticular porque el ion fluoruro (F⁻) es el anión haluro más pequeño, permitiendo una mayor proximidad al catión sodio (Na⁺).

Para ilustrar mejor estos conceptos, observemos la siguiente tabla comparativa con valores aproximados. Nótese que los valores de energía reticular se presentan aquí con signo negativo, correspondiendo a la entalpía de formación de la red.
| Compuesto | Cargas Iónicas | Energía Reticular (kJ/mol) | Punto de Fusión (°C) |
|---|---|---|---|
| LiF | +1, -1 | -1030 | 845 |
| NaCl | +1, -1 | -786 | 801 |
| MgO | +2, -2 | -3795 | 2852 |
| CaCl₂ | +2, -1 | -2258 | 772 |
La tabla muestra claramente cómo el aumento de la carga (comparando MgO con LiF) tiene un efecto drástico en la energía reticular y el punto de fusión, mucho más significativo que las variaciones de tamaño (comparando LiF con NaCl).
Depende de la convención que se utilice. Si hablamos de la energía necesaria para romper la red (proceso de disociación), siempre será un valor positivo porque debemos suministrar energía (endotérmico). Si nos referimos a la energía liberada al formar la red a partir de iones gaseosos, siempre será un valor negativo porque se libera energía (exotérmico). Ambas son correctas, solo describen procesos opuestos.

La relación es directa y muy fuerte. Una mayor energía reticular (en valor absoluto) implica que los iones están unidos más firmemente en la red cristalina. Para fundir el sólido, es necesario aportar suficiente energía térmica para que los iones vibren con la intensidad suficiente como para romper esas uniones. Por lo tanto, a mayor energía reticular, mayor será la temperatura necesaria para alcanzar el punto de fusión.
Es prácticamente imposible crear las condiciones experimentales para medirla directamente. No se puede aislar una cantidad molar de iones en estado gaseoso y luego medir con precisión la energía liberada cuando colapsan para formar un cristal perfecto. Por eso se recurre a métodos indirectos como el ciclo de Born-Haber, que utiliza datos termodinámicos que sí son medibles.
No hay un único “campeón”, pero los compuestos con las energías reticulares más elevadas son aquellos formados por iones pequeños y con cargas muy altas. Compuestos como el óxido de aluminio (Al₂O₃), con iones Al³⁺ y O²⁻, o el nitruro de titanio (TiN), tienen energías reticulares extremadamente elevadas, lo que los convierte en materiales cerámicos muy duros y con puntos de fusión altísimos.

Descubre Q CELLS, el líder mundial en paneles solares. Conoce su historia, la innovación alemana...

Descubre INVAP, la empresa estatal que posiciona a Argentina en la élite tecnológica mundial. Desde...

¿Desapareció tu Panel de Tareas o CommandManager en SolidWorks? ¡No entres en pánico! Aprende a...

Explora el fascinante viaje del Sol a través de la historia: de ser un poderoso...