
Hidrógeno Verde en Chile: La Revolución Energética
Descubre cómo Chile, con su Estrategia Nacional de Hidrógeno Verde, utiliza el poder del sol...
En el complejo mundo de los trasplantes de órganos, el éxito o fracaso de un procedimiento a menudo depende de un delicado equilibrio inmunológico. El principal desafío es evitar que el sistema inmunitario del receptor ataque al nuevo órgano, un fenómeno conocido como rechazo. En el centro de esta batalla se encuentran los anticuerpos anti-HLA, moléculas que pueden predecir y causar el rechazo de un aloinjerto. Durante décadas, los laboratorios han buscado métodos cada vez más precisos y sensibles para detectar estos anticuerpos. Hoy, una tecnología ha emergido como el estándar de oro en muchos centros de trasplante: la técnica Luminex. Este método, basado en microesferas codificadas por colores, no solo ha mejorado drásticamente la sensibilidad y especificidad de la detección, sino que ha redefinido la forma en que evaluamos la compatibilidad entre donante y receptor.
Para entender la importancia de la detección de anticuerpos, primero debemos comprender qué son los Antígenos Leucocitarios Humanos (HLA). Pensemos en los HLA como una especie de “código de barras” molecular presente en la superficie de casi todas nuestras células. Este código es único para cada individuo (excepto en gemelos idénticos) y es la forma en que nuestro sistema inmunitario distingue lo “propio” de lo “extraño”. Cuando se realiza un trasplante, el sistema inmunitario del receptor examina el código de barras HLA del órgano donado. Si las diferencias son significativas, lo identifica como un invasor y desencadena una respuesta inmunitaria para destruirlo. Por esta razón, la compatibilidad HLA entre donante y receptor es un pilar fundamental para el éxito del trasplante.
Un receptor puede desarrollar anticuerpos contra los HLA de otras personas a través de eventos sensibilizantes como embarazos previos (exposición a los HLA paternos del feto), transfusiones de sangre o un trasplante anterior. Estos anticuerpos preformados circulan en la sangre del paciente y, si reconocen los HLA del órgano donado, pueden provocar un rechazo hiperagudo o agudo, a menudo irreversible. La presencia de estos anticuerpos es uno de los mayores factores de riesgo. Por ello, identificarlos con precisión antes del trasplante es una tarea de vital importancia para la seguridad del paciente.
Históricamente, el método principal para detectar anticuerpos era el ensayo de Citotoxicidad Dependiente del Complemento (CDC). Este método enfrentaba linfocitos de un panel de donantes con el suero del receptor. Si había anticuerpos que activaban el complemento, las células morían, indicando una reacción positiva. Sin embargo, el CDC tiene limitaciones significativas:
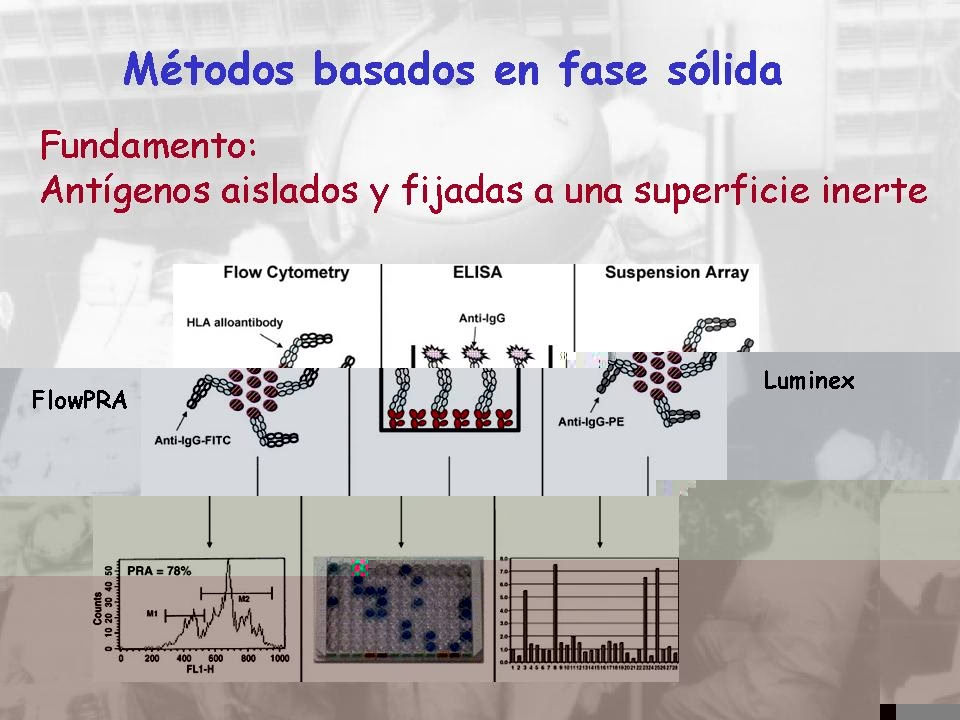
Para superar estas barreras, se desarrollaron métodos de fase sólida como ELISA y la citometría de flujo. Estas técnicas mejoraron la sensibilidad, pero fue la tecnología Luminex la que representó un salto cualitativo, ofreciendo una plataforma multiplexada, de alto rendimiento y con una sensibilidad y especificidad sin precedentes.
El principio fundamental de la tecnología Luminex es su capacidad para analizar simultáneamente múltiples analitos en un solo pozo de reacción. Esto se logra mediante el uso de microesferas de poliestireno. Cada población de microesferas está internamente teñida con una combinación única de dos tintes fluorescentes, creando hasta 100 “colores” o regiones distintas. Esto permite que cada población de microesferas actúe como un portador molecular para un antígeno específico.

El proceso para la detección de anticuerpos anti-HLA se desarrolla en los siguientes pasos:
El software analiza miles de microesferas por segundo, generando un perfil detallado de los anticuerpos específicos que tiene el paciente y su fuerza relativa.
Los ensayos Luminex se presentan principalmente en dos formatos:
| Característica | CDC | ELISA | Luminex (Antígeno Único) |
|---|---|---|---|
| Sensibilidad | Baja | Intermedia-Alta | Muy Alta |
| Especificidad | Limitada (falsos positivos) | Buena | Muy Alta (identifica alelos específicos) |
| Tipo de Anticuerpo | Solo fijadores de complemento | Principalmente IgG | Isotipos específicos (IgG, IgM, etc.) |
| Rendimiento | Bajo, laborioso | Intermedio | Alto (formato de 96 pozos) |
| Información Obtenida | Reactividad general (PRA) | Reactividad general por clase | Perfil detallado de especificidades |
La introducción de Luminex ha transformado la práctica clínica. La capacidad de identificar con precisión el perfil de anticuerpos de un paciente permite una mejor gestión de las listas de espera, evitando ofrecer órganos que serían inmediatamente rechazados. Además, ha dado lugar al concepto de “crossmatch virtual”: en lugar de realizar una prueba física (crossmatch) que consume tiempo, se puede predecir el resultado comparando la lista de anticuerpos inaceptables del receptor (obtenida por Luminex) con el tipaje HLA del donante. Esto es especialmente crucial en el trasplante de riñón de donante fallecido, donde el tiempo es un factor crítico.
Sin embargo, la alta sensibilidad de la técnica también plantea nuevos desafíos. A menudo se detectan anticuerpos a niveles muy bajos, y la relevancia clínica de estos no siempre está clara, generando debates sobre si deben ser considerados una contraindicación para el trasplante. La investigación actual se centra en comprender mejor el impacto de los diferentes isotipos de anticuerpos (IgG1, IgG2, IgG3, IgG4), su capacidad de activar el complemento y su correlación con los resultados a largo plazo del injerto. La tecnología Luminex, por su versatilidad, es una plataforma ideal para llevar a cabo estos estudios y seguir refinando el campo de la histocompatibilidad.
El PRA (Panel Reactive Antibody) es una medida que estima el porcentaje de la población de donantes contra la cual un paciente tiene anticuerpos HLA preformados. Por ejemplo, un PRA del 80% significa que el paciente reaccionaría negativamente contra el 80% de los donantes potenciales, lo que dificulta enormemente encontrar un órgano compatible. Aunque el concepto nació con la técnica CDC, hoy se calcula de forma más precisa (PRA calculado o cPRA) a partir de los datos de especificidad obtenidos con Luminex.

La sensibilidad superior de Luminex se debe a varios factores. Primero, utiliza antígenos HLA purificados y concentrados en las microesferas, aumentando la densidad del objetivo para los anticuerpos. Segundo, la detección por fluorescencia es intrínsecamente más sensible que observar la lisis celular. Finalmente, no depende de la función biológica del anticuerpo (como la activación del complemento), por lo que puede detectar anticuerpos no fijadores de complemento que el CDC pasaría por alto.
No necesariamente. La alta sensibilidad de Luminex puede detectar anticuerpos a niveles muy bajos cuya significancia clínica aún está en debate. La decisión de proceder con un trasplante en presencia de anticuerpos específicos del donante depende de su título (fuerza), su especificidad y la capacidad del centro de trasplantes para manejar el riesgo inmunológico con terapias de desensibilización y un seguimiento post-trasplante riguroso.
Un crossmatch virtual es una predicción del resultado de una prueba de compatibilidad cruzada física. Se basa en comparar dos conjuntos de datos: 1) El perfil detallado de anticuerpos anti-HLA del receptor, identificado mediante la prueba Luminex de Antígeno Único, y 2) El tipaje HLA completo del donante potencial. Si el donante no posee ninguno de los antígenos HLA contra los cuales el receptor tiene anticuerpos, el crossmatch virtual se considera negativo, y es muy probable que el trasplante sea seguro desde el punto de vista inmunológico.

Descubre cómo Chile, con su Estrategia Nacional de Hidrógeno Verde, utiliza el poder del sol...

¿Buscas paneles solares de calidad? Analizamos a Tindo Solar, el único fabricante de Australia. Descubre...
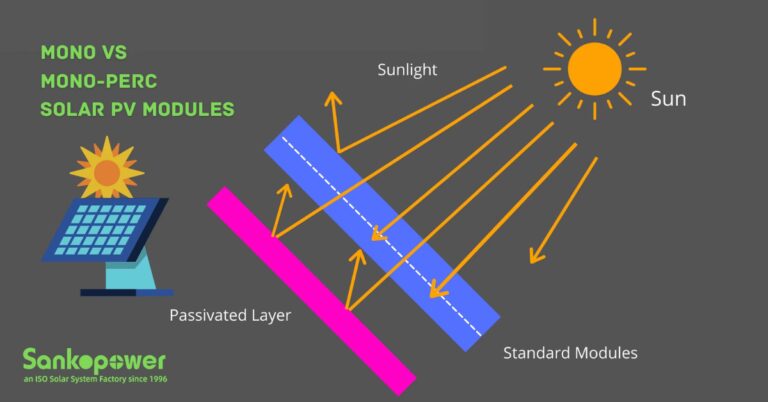
¿Qué son los paneles solares PERC? Descubre cómo esta tecnología revolucionaria aumenta la eficiencia, reduce...
Descubre las mejores aplicaciones para monitorizar tus paneles solares. Controla tu producción, optimiza tu consumo...