
La Cocina Solar Más Grande del Mundo Está en India
Descubre cómo India lidera la revolución de la cocina solar con la instalación más grande...
Todos interactuamos a diario con la materia en sus formas más comunes: el hielo sólido en una bebida, el agua líquida que bebemos y el vapor gaseoso que sale de una tetera. Intuitivamente, sabemos que para pasar de hielo a agua y de agua a vapor necesitamos aplicar calor, es decir, energía. Pero, ¿alguna vez te has detenido a pensar cuál de estos estados contiene más energía? Y más allá de ellos, ¿existe algún estado que supere a todos en cuanto a su nivel energético? La respuesta es un rotundo sí, y nos lleva a un viaje desde lo más quieto y ordenado hasta lo más caótico y poderoso del universo.
Para entender la energía de la materia, debemos pensar a nivel microscópico, en sus partículas fundamentales: átomos y moléculas. El estado en que se encuentra la materia depende directamente de cuánta energía tienen estas partículas para moverse. Es una danza constante entre la energía del movimiento (energía cinética) y las fuerzas que intentan mantener unidas a las partículas (energía potencial).
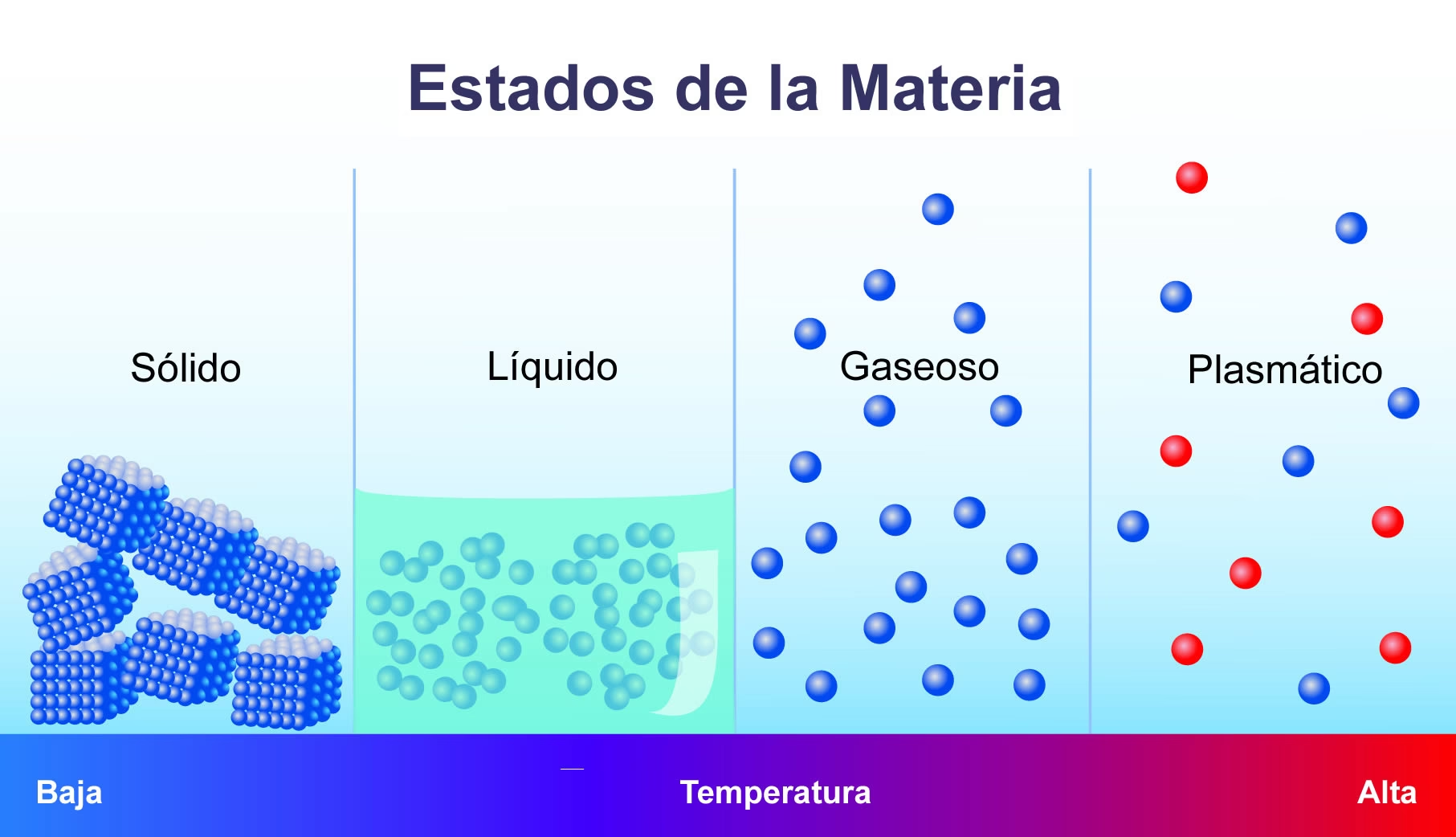
En un sólido, las partículas se encuentran en la escala más baja de energía. Están fuertemente unidas entre sí, formando una estructura rígida y ordenada, como soldados en formación. No tienen la energía suficiente para desplazarse de su posición, pero no están completamente inmóviles. Vibran constantemente en su lugar. Imagina una multitud sentada en un estadio durante un concierto; cada persona (partícula) puede moverse en su asiento, pero no puede correr por el campo. Esta vibración es su energía interna. Por lo tanto, los sólidos son el estado de la materia con la menor cantidad de energía.
Cuando añadimos energía a un sólido, generalmente en forma de calor, sus partículas vibran cada vez con más fuerza. Llega un punto, conocido como punto de fusión, en el que la vibración es tan intensa que las partículas rompen las ataduras rígidas que las mantenían en su lugar. Ahora pueden deslizarse y fluir unas sobre otras. Hemos llegado al estado líquido. Un líquido tiene más energía que un sólido porque sus partículas no solo vibran, sino que también se mueven y chocan entre sí. Siguiendo nuestra analogía, la multitud ha bajado al campo de juego; pueden caminar y mezclarse, pero siguen estando relativamente juntas.
Si continuamos inyectando energía al líquido, sus partículas se moverán cada vez más rápido. En el punto de ebullición, la energía es tan alta que las partículas vencen por completo las fuerzas de atracción que las mantenían unidas. Escapan y se expanden para ocupar todo el volumen del recipiente que las contiene. Esto es un gas. Las partículas de un gas se mueven a grandes velocidades, de forma caótica y con grandes distancias entre ellas. De los tres estados comunes, el gaseoso es el que posee, con diferencia, la mayor cantidad de energía interna. La multitud del concierto ahora ha salido del estadio y corre libremente por un parque inmenso.

Hasta ahora, el gas parece el ganador. Pero, ¿qué sucede si seguimos añadiendo una cantidad de energía verdaderamente colosal a un gas? El resultado es la creación del cuarto y más energético estado de la materia: el plasma. En este estado, la energía es tan descomunal que no solo separa las moléculas, sino que arranca los electrones directamente de los átomos. El resultado ya no es un gas de átomos neutros, sino una especie de “sopa” supercaliente y eléctricamente conductora, formada por iones (átomos que han perdido electrones y tienen carga positiva) y electrones libres.
El plasma es, con diferencia, el estado de la materia con el mayor nivel de energía. Para crearlo, se necesitan temperaturas extremas, como las que se encuentran en el núcleo del Sol y otras estrellas. De hecho, ¡el 99% de la materia visible del universo se encuentra en estado de plasma! No es algo exótico; es la forma más común de la materia a escala cósmica. Aquí en la Tierra, podemos verlo en los rayos de una tormenta, en las auroras boreales, en el fuego y en tecnologías humanas como las luces de neón y los televisores de plasma.
Para visualizar mejor estas diferencias, aquí tienes una tabla que resume las características principales de cada estado en relación con su energía.

| Estado de la Materia | Nivel de Energía Relativo | Movimiento de Partículas | Ejemplos Comunes |
|---|---|---|---|
| Sólido | Muy Bajo | Vibran en una posición fija | Hielo, roca, metal |
| Líquido | Bajo | Se deslizan unas sobre otras | Agua, aceite, mercurio |
| Gas | Alto | Movimiento libre, rápido y aleatorio | Vapor de agua, aire, oxígeno |
| Plasma | Extremadamente Alto | Iones y electrones se mueven caóticamente | El Sol, rayos, auroras boreales |
Es natural que surjan dudas sobre este fascinante tema. A continuación, resolvemos algunas de las más comunes.
La energía interna de una sustancia es la suma de toda la energía contenida en su interior. Se compone principalmente de dos tipos: la energía cinética, que proviene del movimiento y vibración aleatoria de sus partículas, y la energía potencial, que está asociada a las fuerzas intermoleculares que las mantienen unidas. Al calentar una sustancia, aumentamos principalmente su energía cinética, haciendo que sus partículas se muevan más rápido.
Para pasar de líquido a gas, se necesita energía para vencer las fuerzas que unen a las moléculas. Sin embargo, para pasar de gas a plasma, se necesita una cantidad de energía mucho mayor, ya que no solo hay que separar las moléculas, sino que hay que romper los propios átomos, arrancando sus electrones. Este proceso de ionización requiere una entrada de energía masiva, que queda almacenada en el estado de plasma.

No, esto es un error común. El estado sólido tiene energía, aunque sea el nivel más bajo. Sus partículas vibran constantemente. La única situación teórica en la que la materia no tendría energía de movimiento sería en el cero absoluto (-273.15 °C o 0 Kelvin), un punto que, según las leyes de la termodinámica, es inalcanzable.
Sin lugar a dudas, un gas tiene mucha más energía que un sólido. Las partículas de un gas se mueven libremente a altas velocidades y poseen una energía cinética muy superior a las partículas de un sólido, que solo pueden vibrar en su sitio.
La próxima vez que veas un cubito de hielo derritiéndose o el vapor saliendo de una olla, recuerda el increíble viaje energético que está ocurriendo a nivel molecular. La energía no es solo algo que consumimos; es la fuerza fundamental que esculpe la materia, dictando su forma, su comportamiento y su poder. Desde la quietud de un cristal de hielo hasta la furia incandescente de una estrella, la diferencia radica en un solo factor: la cantidad de energía que contienen. Y en esta carrera energética, el plasma reina como el campeón absoluto, recordándonos que el universo está lleno de un poder y un dinamismo que apenas comenzamos a comprender.

Descubre cómo India lidera la revolución de la cocina solar con la instalación más grande...

¿Sabías que el potencial de las energías renovables supera con creces nuestra demanda energética? Descubre...
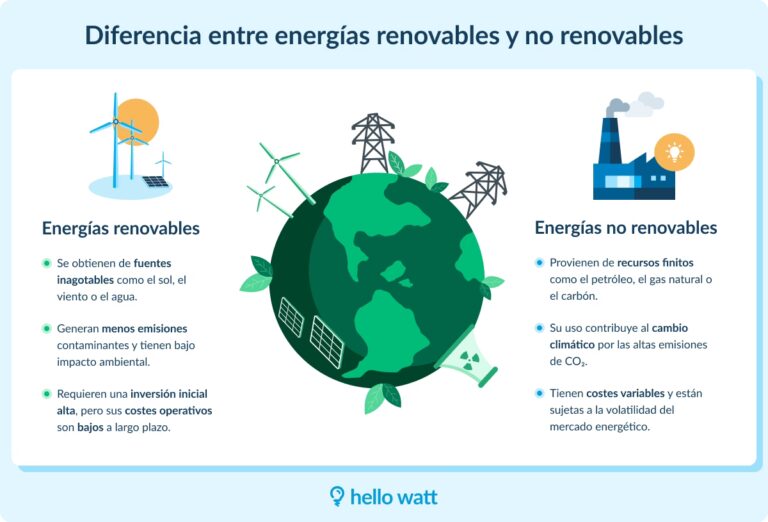
Descubre en qué se diferencia la energía eólica de la solar, hidroeléctrica y otras fuentes...

Descubre la diversificada matriz energética de México. Analizamos las fuentes de energía renovables y no...