
Paneles Solares en Los Ángeles: Guía de Costos 2024
¿Pensando en energía solar en Los Ángeles? Descubre los costos reales, los factores que influyen...
En nuestro día a día, estamos rodeados de dispositivos que dependen de una fuente de energía portátil. Desde el móvil en nuestro bolsillo hasta el control remoto del televisor, todos ellos funcionan gracias a un pequeño milagro de la ingeniería: la batería electroquímica. Pero, ¿alguna vez te has detenido a pensar qué ocurre realmente dentro de esa pequeña caja para que pueda encender una pantalla o mover un motor? La respuesta se encuentra en la fascinante conversión de energía química en energía eléctrica a través de procesos espontáneos que la ciencia ha sabido dominar.
Una batería electroquímica no es más que un dispositivo que aprovecha las reacciones de oxidación-reducción (redox) para generar una corriente eléctrica. En esencia, organiza una transferencia de electrones que, en lugar de ocurrir de forma desordenada, se canaliza a través de un circuito externo para realizar un trabajo útil. A continuación, desglosaremos este proceso, exploraremos sus componentes y descubriremos algunas de las innovaciones más sorprendentes en este campo, incluyendo baterías hechas de papel o activadas por fluidos corporales.
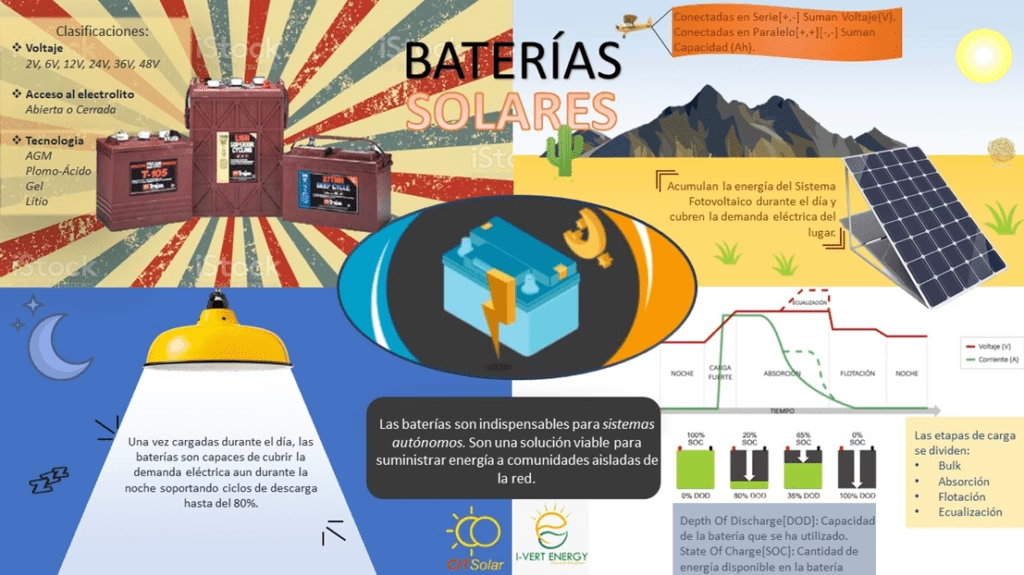
El principio fundamental detrás de cualquier pila o batería es una reacción redox espontánea. Este tipo de reacción involucra dos procesos simultáneos: la oxidación, donde una especie química pierde electrones, y la reducción, donde otra especie los gana. Para que esto se convierta en una fuente de energía, la batería se diseña en dos mitades separadas, llamadas semiceldas.
Este flujo de electrones desde el ánodo hacia el cátodo es lo que conocemos como corriente eléctrica. Sin embargo, para que el sistema funcione, el circuito debe estar cerrado. Aquí es donde entra en juego el electrolito y un componente clave: el puente salino o la membrana de intercambio iónico. Este elemento conecta iónicamente ambas semiceldas, permitiendo que los iones se muevan para equilibrar las cargas generadas por el flujo de electrones, pero evitando que las soluciones de cada semicelda se mezclen y provoquen reacciones secundarias no deseadas.
No cualquier par de materiales puede formar una batería. La reacción redox debe ser espontánea, es decir, debe ocurrir de forma natural liberando energía. Los científicos pueden predecir esto utilizando las tablas de potenciales estándar de reducción. El potencial de la pila (su voltaje) se calcula con una simple fórmula:
Potencial de la pila (ε°) = Potencial del cátodo (ε°cat) – Potencial del ánodo (ε°an)
Si el resultado de esta ecuación es un valor positivo, la reacción es espontánea y la celda electroquímica generará energía eléctrica. Si el resultado es negativo, la reacción no ocurrirá por sí sola y, de hecho, necesitará un aporte de energía externa para forzarla, que es precisamente lo que ocurre cuando recargamos una batería.
Si bien las baterías tradicionales han servido bien a la humanidad, la búsqueda de soluciones más baratas, flexibles, ligeras y ecológicas ha llevado a los investigadores a explorar materiales poco convencionales. Uno de los más prometedores es el papel. Utilizar papel como sustrato o incluso como parte activa de una batería abre un mundo de posibilidades para la electrónica desechable, el empaquetado inteligente y los dispositivos médicos de bajo coste.
El papel puede integrarse en las baterías de dos maneras principales: depositando los electrodos sobre su superficie o utilizando su estructura porosa para contener el electrolito.
| Tipo de Batería | Materiales Clave | Rendimiento Destacado | Aplicación Potencial |
|---|---|---|---|
| Zinc-Aire | Ánodo: Zinc/Carbono, Cátodo: PEDOT | 1.2 V de circuito abierto | Empaquetado inteligente |
| Celulosa-PPy | Fibras de celulosa, Polipirrol (PPy) | Recargable, alta corriente de carga | Almacenamiento de energía flexible |
| Aluminio/Cobre | Ánodo: Al, Cátodo: Cu, Electrolito: Agua | Conexión en serie para 3 V | Electrónica de papel |
| Activada por Orina (Mg/CuCl) | Ánodo: Mg, Cátodo: CuCl | 1.5 V, 1.5 mW (similar a una AA) | Dispositivos médicos de un solo uso |
Una reacción redox (oxidación-reducción) es un proceso químico donde hay una transferencia de electrones. Es el motor fundamental de una batería: la oxidación en el ánodo libera electrones y la reducción en el cátodo los consume. Al forzar a estos electrones a pasar por un circuito externo, se genera la corriente eléctrica.

No. Para que una batería produzca energía, la reacción redox debe ser espontánea, lo que significa que libera energía de forma natural. Esto se determina calculando el potencial de la celda. Si el potencial es positivo, la reacción es espontánea y puede usarse para generar electricidad.
El papel es un material de bajo costo, abundante, ligero, flexible y biodegradable. Usarlo para fabricar baterías podría reducir drásticamente el costo y el impacto ambiental de la electrónica desechable, como sensores médicos, etiquetas inteligentes o dispositivos de diagnóstico para zonas con recursos limitados.
El electrolito es una sustancia (generalmente un líquido o un gel) que contiene iones libres y actúa como medio conductor de la electricidad dentro de la batería. Su función es permitir el movimiento de iones entre el cátodo y el ánodo para mantener el equilibrio de cargas, cerrando así el circuito eléctrico sin que los electrodos se toquen.
Las baterías electroquímicas son mucho más que simples componentes de nuestros aparatos. Son el resultado de una profunda comprensión de la química, que nos permite convertir reacciones a nivel molecular en energía útil y controlable. Desde los principios básicos de la oxidación y la reducción hasta la frontera de la innovación con materiales como el papel, este campo no deja de evolucionar.
La investigación en baterías más eficientes, baratas y sostenibles es crucial para el futuro de la tecnología, desde la electrónica portátil hasta los sistemas de almacenamiento de energía a gran escala. La próxima vez que enciendas tu teléfono, recuerda la compleja y elegante danza de electrones e iones que lo hace posible, un proceso que sigue inspirando a los científicos a crear un futuro más sostenible y energéticamente inteligente.

¿Pensando en energía solar en Los Ángeles? Descubre los costos reales, los factores que influyen...
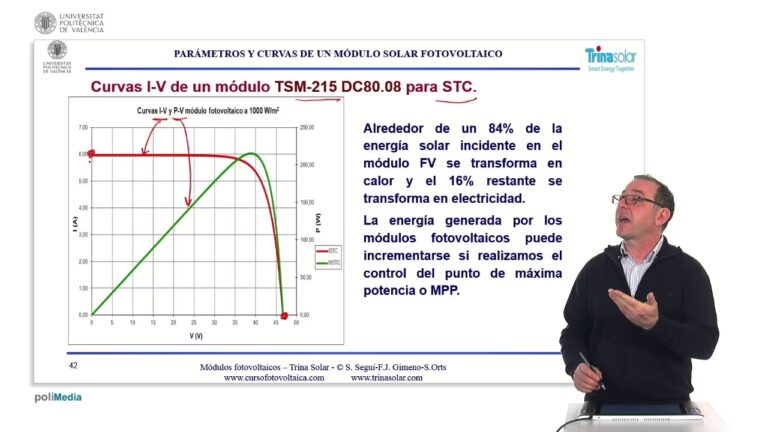
Descubre qué es la curva característica I-V de un panel solar. Entiende cómo este 'ADN...

¿Buscas la mejor forma de calefaccionar tu hogar? Analizamos las estufas a pellets, paneles eléctricos...

Descubre qué es la biomasa, cómo transforma residuos orgánicos en calor y electricidad de forma...