
EPC Solar: Contrato vs. Certificado Energético
El término EPC en energía solar tiene dos significados clave. Descubre la diferencia entre un...
En el vasto mundo de la química orgánica, los compuestos carbonílicos, como los aldehídos y las cetonas, ocupan un lugar central debido a su reactividad y presencia en innumerables procesos biológicos e industriales. Una de las diferencias más notables y fundamentales entre estos dos grupos funcionales es su comportamiento frente a la oxidación. Mientras que los aldehídos se oxidan con relativa facilidad, las cetonas son famosas por su resistencia a este tipo de reacciones. Esta guía completa explora en profundidad por qué existe esta diferencia, bajo qué condiciones se puede oxidar una cetona y cómo esta propiedad se utiliza para distinguirlas en el laboratorio.
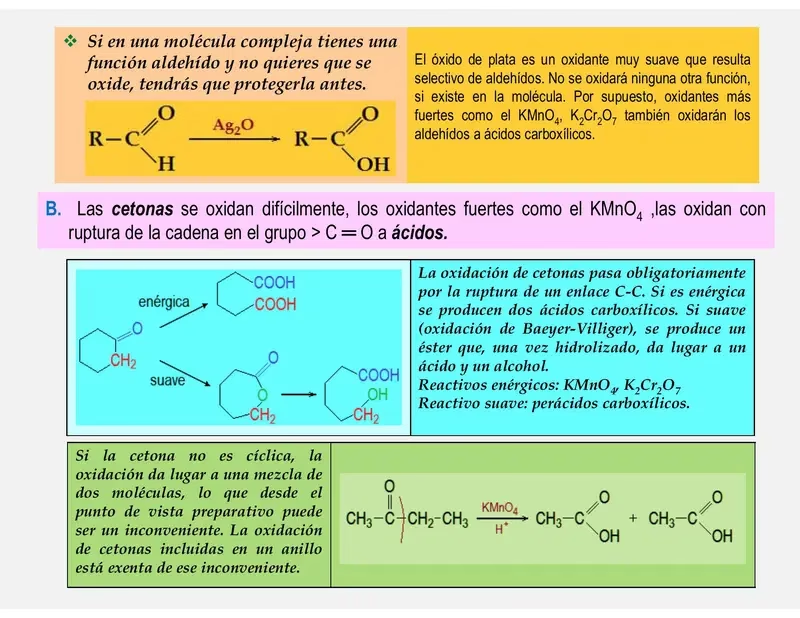
Para entender por qué los aldehídos y las cetonas se comportan de manera tan diferente, primero debemos observar su estructura. Ambos contienen un grupo carbonilo (un átomo de carbono unido por un doble enlace a un átomo de oxígeno, C=O). La diferencia radica en los átomos o grupos unidos a este carbono carbonílico.
Esta aparentemente pequeña diferencia, la presencia de un átomo de hidrógeno directamente unido al carbono carbonílico en los aldehídos, es la razón principal de su facilidad de oxidación. Este enlace C-H es susceptible a la ruptura por agentes oxidantes, permitiendo que el aldehído se convierta en un ácido carboxílico (R-COOH). Las cetonas, al carecer de este hidrógeno, no tienen una vía de reacción tan sencilla. Para oxidar una cetona, se requeriría la ruptura de un enlace carbono-carbono (C-C), que es mucho más fuerte y estable, y por lo tanto, requiere condiciones mucho más energéticas y drásticas.
La distinta reactividad frente a la oxidación es la base de varias pruebas químicas clásicas utilizadas para diferenciar aldehídos de cetonas. Estas pruebas emplean agentes oxidantes suaves que son capaces de reaccionar con los aldehídos pero dejan intactas a las cetonas.
Una de las pruebas más icónicas es la que utiliza el reactivo de Tollens. Este reactivo es una solución amoniacal de nitrato de plata, que contiene el ion complejo diaminaplata(I), [Ag(NH₃)₂]⁺.
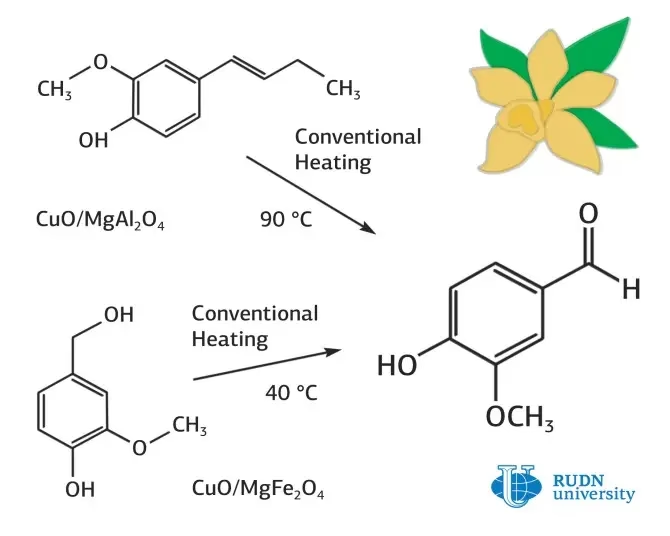
Cuando un aldehído se calienta suavemente con el reactivo de Tollens recién preparado, ocurre una reacción de óxido-reducción. El aldehído se oxida al anión carboxilato correspondiente (ya que la reacción ocurre en medio alcalino), mientras que los iones de plata(I) se reducen a plata metálica (Ag). Esta plata elemental se deposita en las paredes internas del tubo de ensayo, formando una capa reflectante y brillante, similar a un espejo. Este resultado positivo es característico de los aldehídos.
La ecuación general de la reacción es:
R-CHO + 2[Ag(NH₃)₂]⁺ + 3OH⁻ → R-COO⁻ + 2Ag(s) + 4NH₃ + 2H₂O
Las cetonas, por otro lado, no reaccionan con el reactivo de Tollens bajo estas condiciones, por lo que la solución incolora no sufre ningún cambio. Esta prueba es tan fiable que se conoce comúnmente como la “prueba del espejo de plata”.
Ambas soluciones son variantes de un mismo principio y contienen iones de cobre(II) (Cu²⁺) complejados en una solución alcalina. La solución de Fehling utiliza iones tartrato para complejar el cobre, mientras que la de Benedict usa iones citrato. En ambos casos, el reactivo tiene un color azul intenso característico.
Al calentar un aldehído con cualquiera de estos reactivos, el aldehído se oxida a anión carboxilato. Simultáneamente, los iones de cobre(II) de color azul se reducen a óxido de cobre(I) (Cu₂O), que es un sólido insoluble de color rojo ladrillo o marrón rojizo. La aparición de este precipitado es una prueba positiva para un aldehído.
La ecuación simplificada es:
R-CHO + 2Cu²⁺(complejado) + 5OH⁻ → R-COO⁻ + Cu₂O(s) + 3H₂O
Nuevamente, las cetonas no reaccionan, y la solución permanece azul. Es importante destacar que los aldehídos aromáticos generalmente no dan positivo en la prueba de Fehling.

| Prueba | Reactivo Principal | Resultado con Aldehído | Resultado con Cetona |
|---|---|---|---|
| Prueba de Tollens | Ion diaminaplata(I), [Ag(NH₃)₂]⁺ | Formación de un espejo de plata. | Sin reacción (la solución permanece incolora). |
| Prueba de Fehling | Ion cobre(II) complejado con tartrato. | Formación de un precipitado rojo ladrillo (Cu₂O). | Sin reacción (la solución permanece azul). |
| Prueba de Benedict | Ion cobre(II) complejado con citrato. | Formación de un precipitado rojo ladrillo (Cu₂O). | Sin reacción (la solución permanece azul). |
A pesar de su resistencia, no es correcto afirmar que las cetonas no se pueden oxidar en absoluto. Pueden ser oxidadas, pero solo bajo condiciones vigorosas. Esto implica el uso de agentes oxidantes muy fuertes, como el permanganato de potasio (KMnO₄) o el dicromato de potasio (K₂Cr₂O₇) en medio ácido, y a temperaturas elevadas.
Bajo estas condiciones extremas, la oxidación de las cetonas es un proceso destructivo. En lugar de una simple conversión, la reacción provoca la ruptura de los enlaces carbono-carbono adyacentes al grupo carbonilo. Como resultado, la molécula de cetona se fragmenta, produciendo una mezcla de ácidos carboxílicos con un número menor de átomos de carbono que la cetona original.
Por ejemplo, la oxidación de una cetona asimétrica como la 2-pentanona puede romper el enlace C-C a cada lado del grupo carbonilo, dando lugar a diferentes mezclas de productos. Este tipo de reacción es mucho menos “limpia” y controlada que la oxidación de los aldehídos, y por lo tanto, tiene menos utilidad sintética.
Irónicamente, aunque las cetonas son difíciles de oxidar, ellas mismas se forman a través de una reacción de oxidación. Específicamente, las cetonas son el producto de la oxidación de alcoholes secundarios. Utilizando agentes oxidantes como el ácido crómico (H₂CrO₄, reactivo de Jones) o el permanganato de potasio, un alcohol secundario (donde el carbono que lleva el grupo -OH está unido a otros dos carbonos) se convierte eficientemente en una cetona. Esta reacción es fundamental en la síntesis orgánica para preparar cetonas a partir de sus precursores alcohólicos.
La diferencia fundamental es que los aldehídos tienen un átomo de hidrógeno unido directamente al carbono del grupo carbonilo (enlace C-H). Este enlace es relativamente fácil de oxidar. Las cetonas carecen de este hidrógeno; en su lugar, tienen dos enlaces carbono-carbono (C-C), que son mucho más fuertes y resistentes a la oxidación.
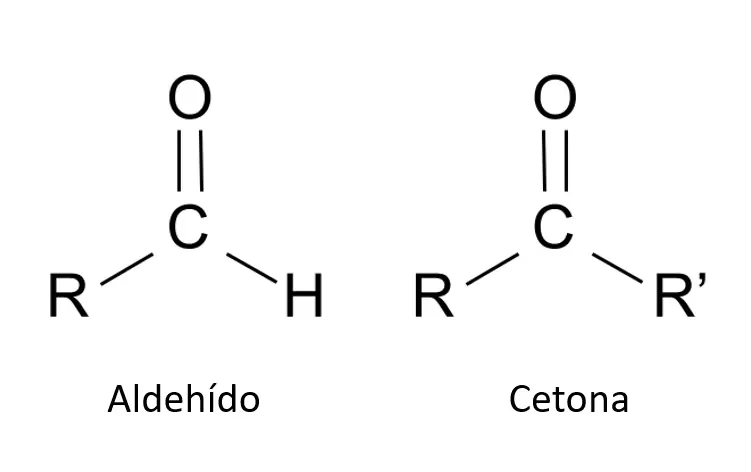
La prueba del espejo de plata utiliza el reactivo de Tollens, que es un agente oxidante suave. Es lo suficientemente fuerte como para reaccionar con el enlace C-H del aldehído, pero no tiene la energía suficiente para romper los robustos enlaces C-C de una cetona. Por eso, solo los aldehídos dan un resultado positivo.
Se requieren condiciones drásticas o vigorosas. Esto incluye el uso de agentes oxidantes muy potentes (como el permanganato de potasio en caliente y en medio ácido) y temperaturas elevadas. Estas condiciones proporcionan la energía necesaria para romper los enlaces carbono-carbono de la molécula.
La oxidación de una cetona es un proceso destructivo que fragmenta la molécula. El resultado es una mezcla de ácidos carboxílicos, cada uno con menos átomos de carbono que la cetona de partida. La composición exacta de la mezcla depende de la estructura de la cetona original.
La resistencia de las cetonas a la oxidación en comparación con los aldehídos es una de las lecciones fundamentales de la química de los compuestos carbonílicos. Esta diferencia, arraigada en su estructura molecular, no solo define gran parte de su reactividad química, sino que también proporciona una base práctica para su identificación en el laboratorio. Si bien los aldehídos sucumben fácilmente a agentes oxidantes suaves, las cetonas se mantienen firmes, cediendo solo ante ataques químicos vigorosos y destructivos que rompen su esqueleto de carbono. Comprender esta dinámica es esencial para cualquier persona que se adentre en el estudio o la aplicación de la química orgánica.

El término EPC en energía solar tiene dos significados clave. Descubre la diferencia entre un...

¿Pensando en instalar paneles solares? No todos son iguales. Descubre por qué un sistema barato...
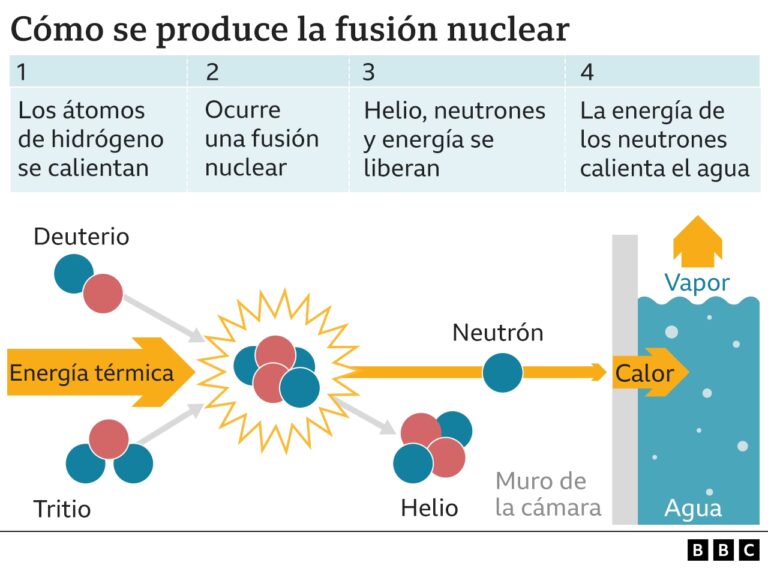
Descubre si la fusión nuclear es la energía renovable definitiva. ¿Cómo funciona, qué combustibles utiliza...

Descubre el costo de instalar paneles solares en tu hogar en Colombia, desde $4 millones....