
Baterías de Litio vs. Plomo-Ácido: ¿Cuál dura más?
Descubre la batalla tecnológica entre las baterías de Ion de Litio y Plomo-Ácido. Analizamos su...
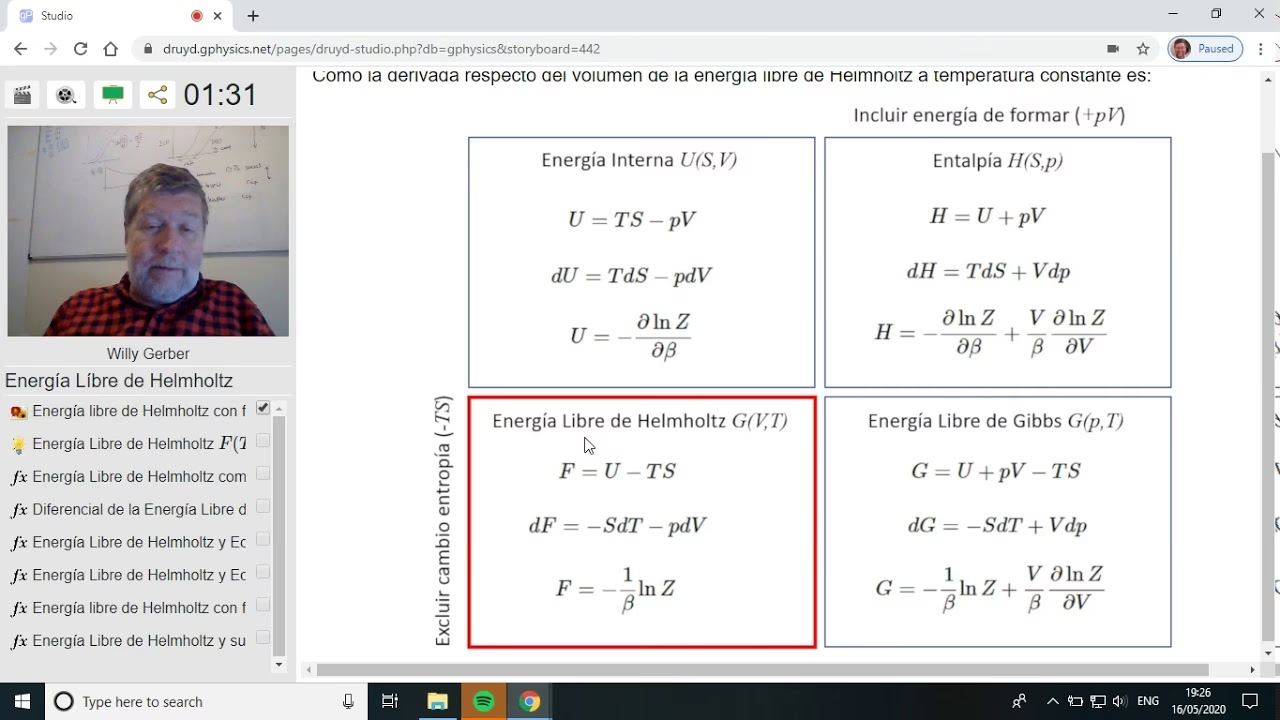
En el vasto universo de la termodinámica, existen conceptos que son fundamentales para entender cómo la energía se transforma y se utiliza. Uno de los más importantes, aunque a veces menos conocido que su contraparte de Gibbs, es la energía libre de Helmholtz. Nombrada en honor al brillante médico y físico alemán Hermann von Helmholtz (1821-1894), esta magnitud nos ofrece una ventana para comprender la cantidad de energía que un sistema cerrado puede convertir en trabajo útil bajo condiciones muy específicas: a temperatura y volumen constantes. Es, en esencia, una medida del potencial de un sistema para realizar cambios.
Imagina que tienes un sistema con una cantidad total de energía, conocida como energía interna. Sin embargo, no toda esa energía está disponible para que la uses a tu antojo. Una parte está intrínsecamente ligada al desorden y al movimiento aleatorio de las partículas, un concepto que conocemos como entropía. La energía libre de Helmholtz es precisamente lo que queda cuando restamos esta energía “caótica” o “no disponible” de la energía total. Nos dice cuánta energía está realmente “libre” para efectuar un trabajo.

La energía libre de Helmholtz, representada comúnmente con la letra A (del alemán “Arbeit”, que significa trabajo) o a veces F, es un potencial termodinámico. Su propósito principal es determinar la espontaneidad de un proceso que ocurre en un sistema cerrado, a temperatura constante (isotérmico) y a volumen constante (isocórico). En palabras más sencillas, nos ayuda a predecir si una reacción química o un proceso físico ocurrirá por sí solo en un recipiente sellado y rígido que se mantiene a una temperatura fija.
El concepto clave aquí es el de “trabajo útil máximo”. La disminución en la energía libre de Helmholtz durante un proceso reversible a T y V constantes es igual al máximo trabajo que el sistema puede realizar sobre su entorno. Por esta razón, históricamente también se le conocía como la “función de trabajo”.

La definición matemática de la energía libre de Helmholtz es elegante y poderosa. Nos permite cuantificar este potencial con una simple ecuación:
A = U – TS
Para entenderla completamente, desglosemos sus componentes:
El término TS representa la cantidad de energía que está “atada” al desorden térmico del sistema y que, por lo tanto, no está disponible para realizar un trabajo útil. Al restar este término de la energía interna total (U), obtenemos la energía que sí está disponible (A).
En termodinámica, los valores absolutos suelen ser menos importantes que los cambios. El cambio en la energía libre de Helmholtz (ΔA) durante un proceso nos dice si este ocurrirá de forma espontánea:
ΔA = ΔU – TΔS (para un proceso a temperatura constante)
La interpretación del signo de ΔA es crucial:
Por ejemplo, consideremos una reacción química en un reactor sellado a 300 K. Si el cambio en la energía interna (ΔU) es de -500 Julios y el cambio en la entropía (ΔS) es de -1 J/K, podemos calcular ΔA:
ΔA = (-500 J) – (300 K * -1 J/K) = -500 J + 300 J = -200 J
Como ΔA es negativo (-200 J), la reacción ocurrirá espontáneamente bajo estas condiciones de temperatura y volumen constantes.
Aunque la energía libre de Gibbs es más comúnmente utilizada en química (ya que muchas reacciones ocurren a presión constante), la energía de Helmholtz es indispensable en varios campos de la física y la ciencia de materiales donde las condiciones de volumen constante son la norma.
| Campo de Aplicación | Descripción de Uso |
|---|---|
| Ciencia de Materiales | Se utiliza para modelar el comportamiento de sólidos bajo deformación. La energía libre se puede descomponer en contribuciones elásticas y plásticas para entender cómo un material almacena y disipa energía. |
| Mecánica Estadística | Es un puente fundamental entre el mundo microscópico de las partículas y el mundo macroscópico de la termodinámica. Se relaciona directamente con la función de partición, una herramienta matemática que permite calcular todas las propiedades termodinámicas de un sistema a partir de sus estados de energía moleculares. |
| Termodinámica de Mezclas | Sirve para calcular los cambios de energía durante la mezcla de sustancias o las transiciones de fase (como la solidificación o evaporación) que ocurren en un volumen fijo. |
| Física de Polímeros | Ayuda a describir el comportamiento complejo de los polímeros cuando se estiran o deforman, separando las contribuciones energéticas de la elasticidad, la plasticidad y la viscosidad. |
Es común confundir la energía libre de Helmholtz (A) con la energía libre de Gibbs (G). La diferencia fundamental radica en las condiciones bajo las cuales cada una es aplicable. Ambas miden la energía disponible para trabajo, pero en escenarios distintos.
| Característica | Energía Libre de Helmholtz (A) | Energía Libre de Gibbs (G) |
|---|---|---|
| Condiciones Constantes | Temperatura (T) y Volumen (V) | Temperatura (T) y Presión (P) |
| Representa | El máximo trabajo útil total que puede realizar un sistema. | El máximo trabajo útil no expansivo (trabajo que no sea de expansión/compresión P-V). |
| Fórmula | A = U – TS | G = H – TS (donde H es la entalpía, H = U + PV) |
| Escenario Típico | Una reacción química en un calorímetro de bomba (un recipiente rígido y sellado). | Una reacción química en un vaso de precipitados abierto a la atmósfera. |
Es imposible hablar de esta energía sin mencionar a su creador, Hermann von Helmholtz. Fue una de las mentes más brillantes del siglo XIX, cuyas contribuciones abarcaron una asombrosa variedad de campos. Además de sus trabajos en termodinámica, que llevaron a la formulación del principio de conservación de la energía, Helmholtz hizo aportes revolucionarios en:
Es una propiedad extensiva. Esto significa que su valor es directamente proporcional a la cantidad de materia en el sistema. Si duplicas la masa del sistema manteniendo las mismas condiciones, la energía libre de Helmholtz también se duplicará.
Se le llama “libre” porque representa la porción de la energía interna total de un sistema que está disponible o “liberada” para ser convertida en trabajo mecánico o de otro tipo durante un proceso a temperatura constante. La otra parte, T*S, está “atrapada” en el desorden del sistema.

La energía interna (U) es la energía total de un sistema. La energía libre de Helmholtz (A) es una parte de esa energía interna. Específicamente, es la energía interna menos la energía asociada al desorden entrópico (TS). Por lo tanto, A siempre será menor que U (para T > 0) y representa la fracción de U que es termodinámicamente útil para realizar trabajo.
La elección depende de las restricciones del proceso que estés analizando. Debes usar la energía libre de Helmholtz cuando el proceso se lleva a cabo a volumen constante y temperatura constante. En cambio, si el proceso ocurre a presión constante y temperatura constante (un escenario mucho más común en laboratorios de química), la energía libre de Gibbs es la herramienta adecuada.

Descubre la batalla tecnológica entre las baterías de Ion de Litio y Plomo-Ácido. Analizamos su...

Descubre la sorprendente relación entre los paneles solares y la tecnología láser. ¿Pueden los láseres...
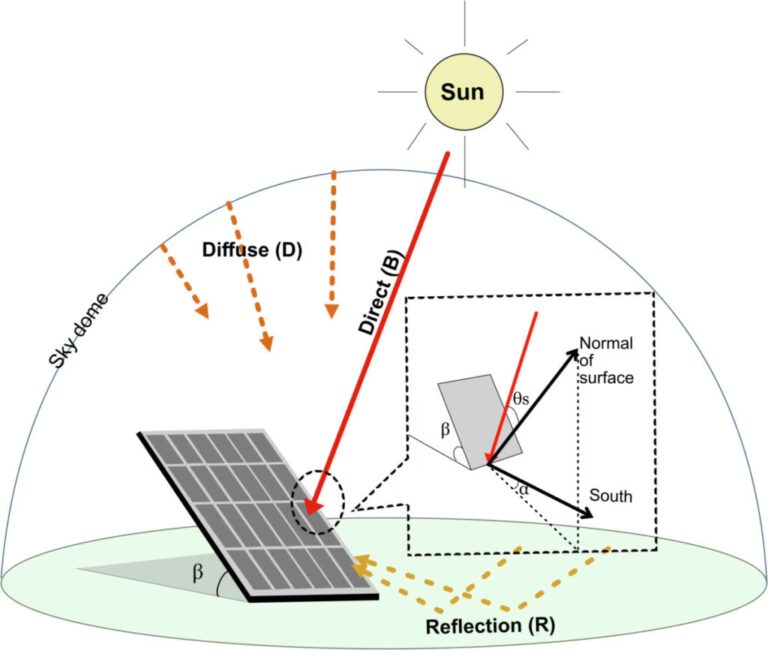
¿Quieres maximizar la energía de tus paneles solares en Argentina? Descubre la inclinación y orientación...

Descubre cómo instalar paneles solares en tu autocaravana paso a paso. Desde la fijación de...