
Energía Solar: La Inversión Inteligente y Sostenible
Descubre cómo el Vaticano se alimenta 100% con energía solar y cómo puedes aplicar la...
En el fascinante mundo de la química, existen fuerzas invisibles que gobiernan la estructura y las propiedades de la materia. Una de las más poderosas y fundamentales en los compuestos iónicos es la energía reticular. Podríamos pensar en ella como el “pegamento” o la energía cohesiva que mantiene unidos a los iones en una estructura cristalina ordenada y rígida, como la de la sal de mesa. Es una medida directa de la fuerza de los enlaces iónicos y, por lo tanto, un concepto clave para entender por qué algunos cristales son increíblemente duros y otros se disuelven con facilidad.
Esta energía representa la cantidad de energía que se necesita para desmantelar por completo un mol de un compuesto iónico sólido y convertirlo en sus iones constituyentes en estado gaseoso, infinitamente separados unos de otros. Imagina tener que romper cada una de las atracciones entre los iones positivos (cationes) y negativos (aniones) en un cristal; la energía total que invertirías en ese proceso es, precisamente, la energía reticular. Al ser una energía que debemos suministrar, siempre tiene un valor positivo.

La definición más aceptada y utilizada de energía reticular (U) es un proceso endotérmico, es decir, que requiere energía. Se visualiza con la siguiente reacción genérica para un compuesto como el cloruro de sodio (NaCl):
NaCl(s) → Na⁺(g) + Cl⁻(g)
La energía requerida para que esta reacción ocurra en un mol de NaCl es de +786 kJ. Este valor positivo nos indica la enorme estabilidad de la red cristalina; se necesita una cantidad considerable de energía para romperla.
Sin embargo, es importante saber que algunas fuentes definen este concepto de manera opuesta: como la energía que se libera cuando los iones gaseosos se unen para formar un mol del sólido iónico (un proceso exotérmico). En ese caso, el valor sería negativo (-786 kJ/mol para el NaCl). Aunque ambas definiciones describen el mismo fenómeno desde perspectivas opuestas, la convención de la energía requerida para romper el cristal (valor positivo) es la más extendida en la química moderna.
La fuerza de esta “unión iónica” no es la misma para todos los compuestos. Depende fundamentalmente de dos factores que se derivan de la ley de Coulomb, la cual describe la fuerza electrostática entre partículas cargadas. La energía reticular se puede calcular teóricamente con una ecuación modificada:
U ∝ (Q₁ * Q₂) / r₀
Donde Q₁ y Q₂ son las cargas de los iones y r₀ es la distancia entre sus núcleos. Analicemos estos dos pilares:
Este es el factor más influyente. La energía reticular es directamente proporcional al producto de las cargas iónicas. A mayor carga en los iones, la atracción electrostática será mucho más fuerte y, por ende, la energía reticular será significativamente mayor.
Aunque los tamaños de los iones son comparables, al duplicar las cargas de ambos iones, la energía reticular se cuadruplica aproximadamente. Esto explica por qué el MgO es mucho más duro y tiene un punto de fusión mucho más alto (2852 °C) que el NaF (993 °C).
Este factor se relaciona con el tamaño de los iones. La energía reticular es inversamente proporcional a la distancia internuclear (la suma del radio iónico del catión y el anión). Iones más pequeños pueden acercarse más entre sí, lo que resulta en una distancia (r₀) menor y una atracción electrostática más intensa.
Un hecho curioso de la energía reticular es que no se puede medir directamente en un laboratorio. Es imposible tomar un cristal de sal y medir la energía exacta para separarlo en iones gaseosos. Sin embargo, podemos calcularla de forma indirecta y muy precisa utilizando el Ciclo de Born-Haber.
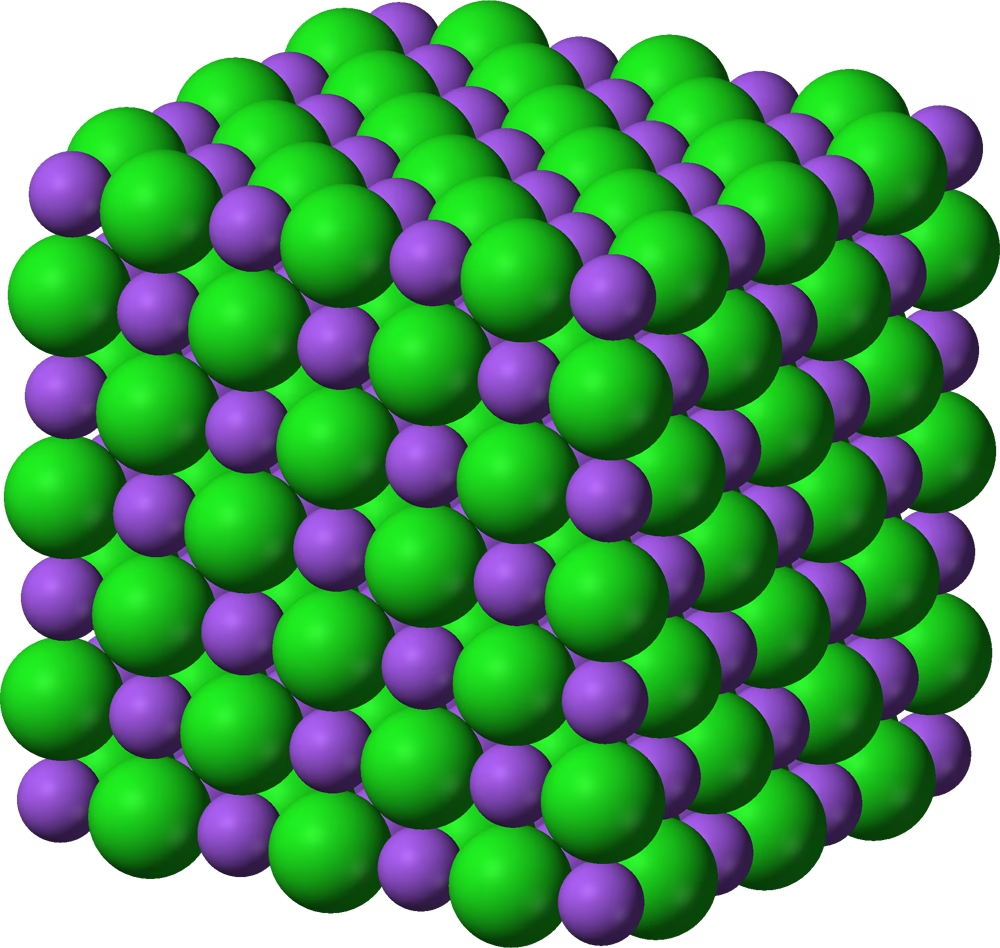
Este ciclo es una aplicación ingeniosa de la Ley de Hess, que establece que el cambio total de energía en una reacción química es el mismo, sin importar el camino que se tome. El ciclo descompone la formación de un compuesto iónico en una serie de pasos hipotéticos cuyas energías sí podemos medir:
Conociendo los valores de todos estos pasos, la energía reticular es la pieza que falta en el rompecabezas energético. Al sumar todas las energías del ciclo, podemos despejar y encontrar el valor de U.
La energía reticular no es solo un número teórico; tiene consecuencias directas y observables en las propiedades de los compuestos iónicos.
| Sustancia | Energía Reticular (U) en kJ/mol | Análisis de los Factores |
|---|---|---|
| NaI | 682 | Cargas bajas (+1, -1) y un anión grande (I⁻), lo que resulta en una energía relativamente baja. |
| CaI₂ | 1971 | La carga del catión es +2 (Ca²⁺), lo que aumenta drásticamente la energía en comparación con el NaI. |
| MgI₂ | 2293 | Similar al CaI₂, pero el Mg²⁺ es más pequeño que el Ca²⁺, lo que reduce la distancia y aumenta aún más la energía. |
| Na₂O | 2481 | La carga del anión es -2 (O²⁻), un factor dominante que eleva mucho la energía. |
| CaCO₃ | 2804 | Iones con carga +2 (Ca²⁺) y -2 (CO₃²⁻), lo que conduce a una energía reticular muy alta. |
Según la convención más utilizada, sí. Representa la energía que se debe suministrar para romper la red cristalina, por lo que es un proceso endotérmico con un valor positivo. Si se define como la energía liberada durante la formación de la red, entonces sería negativa.
Teóricamente, un compuesto formado por los iones más pequeños posibles con las cargas más altas posibles. Por ejemplo, compuestos como el nitruro de aluminio (AlN), con iones Al³⁺ y N³⁻, tienen energías reticulares extremadamente altas.
Son conceptos muy similares. La energía reticular (ΔU) y la entalpía reticular (ΔH) están relacionadas por la ecuación ΔH = ΔU + pΔV. Para sólidos, el cambio de volumen (ΔV) es muy pequeño, por lo que la diferencia entre ambas es mínima y a menudo se usan indistintamente en contextos introductorios.
En conclusión, la energía reticular es mucho más que un simple valor en una tabla; es la medida cuantitativa de la estabilidad de un compuesto iónico. Comprender los factores que la gobiernan —la carga y el tamaño de los iones— nos permite predecir y explicar propiedades fundamentales como la dureza, el punto de fusión y la solubilidad, revelando la poderosa arquitectura que subyace en el mundo cristalino.

Descubre cómo el Vaticano se alimenta 100% con energía solar y cómo puedes aplicar la...
¿Pensando en conectar un panel solar directamente a tu batería de litio? ¡Detente! Descubre por...

¿Vale la pena invertir en paneles solares? Analizamos a fondo el retorno de la inversión...

Descubre qué es la energía renovable marina y cómo las olas, mareas y corrientes oceánicas...