
Granjas Solares: ¿Qué son y cómo funcionan?
Descubre qué es una granja solar, también llamada huerto o parque fotovoltaico. Te explicamos cómo...
En el corazón de toda la materia que nos rodea, desde el aire que respiramos hasta los avanzados paneles solares que convierten la luz en electricidad, se encuentra el átomo. Y dentro de este diminuto universo, los electrones danzan en una coreografía precisa dictada por las leyes de la física cuántica. Lejos de ser un simple sistema planetario en miniatura, la estructura atómica es un complejo sistema de probabilidades y energías. El concepto clave para entender este comportamiento es el de los niveles de energía. Estos niveles no son órbitas físicas, sino regiones de probabilidad con energías específicas y cuantizadas donde es más probable encontrar un electrón. Comprenderlos es fundamental para desentrañar los secretos de la química, la electricidad y la generación de energía.
Imagina un edificio de apartamentos de siete pisos. Un residente puede estar en el primer piso, en el segundo o en el séptimo, pero nunca podrá vivir en el piso 2.5. Los niveles de energía de un átomo funcionan de manera similar. Un electrón puede ocupar un nivel de energía específico, pero no puede existir en los espacios intermedios. A esto se le llama cuantización de la energía. Cada uno de estos niveles representa una cantidad fija de energía que un electrón puede poseer. Los niveles más cercanos al núcleo atómico (cargado positivamente) son los de menor energía. Para que un electrón salte a un nivel superior, más alejado del núcleo, necesita absorber una cantidad exacta de energía. A la inversa, cuando un electrón “cae” a un nivel inferior, libera esa misma cantidad de energía, a menudo en forma de un fotón de luz.
En la teoría atómica, se describen siete niveles principales de energía, numerados del 1 al 7. Estos también se conocen como capas o niveles cuánticos principales (designados con la letra ‘n’). Cada nivel tiene una capacidad máxima de electrones que puede albergar.
Es importante destacar que no todos los átomos utilizan los siete niveles. Un átomo de hidrógeno, con un solo electrón, ocupará en su estado fundamental únicamente el Nivel 1. A medida que los átomos tienen más electrones (como el Uranio, con 92), van llenando progresivamente estos niveles de energía.
Para complicar un poco más el modelo, cada nivel principal de energía (excepto el primero) se subdivide en subniveles. Estos subniveles corresponden a diferentes formas de orbitales atómicos, que son las regiones tridimensionales donde la probabilidad de encontrar un electrón es máxima. Hay cuatro tipos de subniveles, designados con las letras s, p, d y f.
La distribución no es arbitraria; sigue un patrón definido:
| Nivel Principal (n) | Subniveles Presentes | Máximo de Electrones |
|---|---|---|
| 1 | s | 2 |
| 2 | s, p | 8 (2 + 6) |
| 3 | s, p, d | 18 (2 + 6 + 10) |
| 4 | s, p, d, f | 32 (2 + 6 + 10 + 14) |
La forma en que los electrones llenan estos subniveles se conoce como configuración electrónica, un mapa que nos dice la “dirección” exacta de cada electrón en el átomo.
Un electrón en un átomo posee dos tipos de energía que definen su estado. Primero, tiene energía potencial. Esta energía surge de la atracción electrostática entre la carga negativa del electrón y la carga positiva del núcleo. Cuanto más cerca está el electrón del núcleo, mayor es esta fuerza de atracción y menor es su energía potencial. Segundo, el electrón posee energía cinética, que se deriva de su movimiento o, más precisamente, de su naturaleza ondulatoria dentro del orbital. La suma de estas dos energías da la energía total del electrón en ese nivel, y es esta energía total la que está cuantizada.
Los electrones pueden moverse entre estos niveles de energía, pero no de forma gradual. Este movimiento, conocido como transición o salto cuántico, es instantáneo. Para que un electrón salte de un nivel de energía inferior a uno superior, debe absorber la cantidad exacta de energía que corresponde a la diferencia entre ambos niveles. Esta energía puede provenir de la colisión con otra partícula o, más comúnmente, de la absorción de un fotón de luz. De manera similar, un electrón en un estado “excitado” (en un nivel de energía más alto de lo normal) tenderá a regresar a su nivel fundamental, más estable. Al hacerlo, emite la energía sobrante, generalmente como un fotón de luz con una longitud de onda (y por tanto, un color) muy específica. Este principio es la base de la espectroscopia, los láseres y las luces de neón.
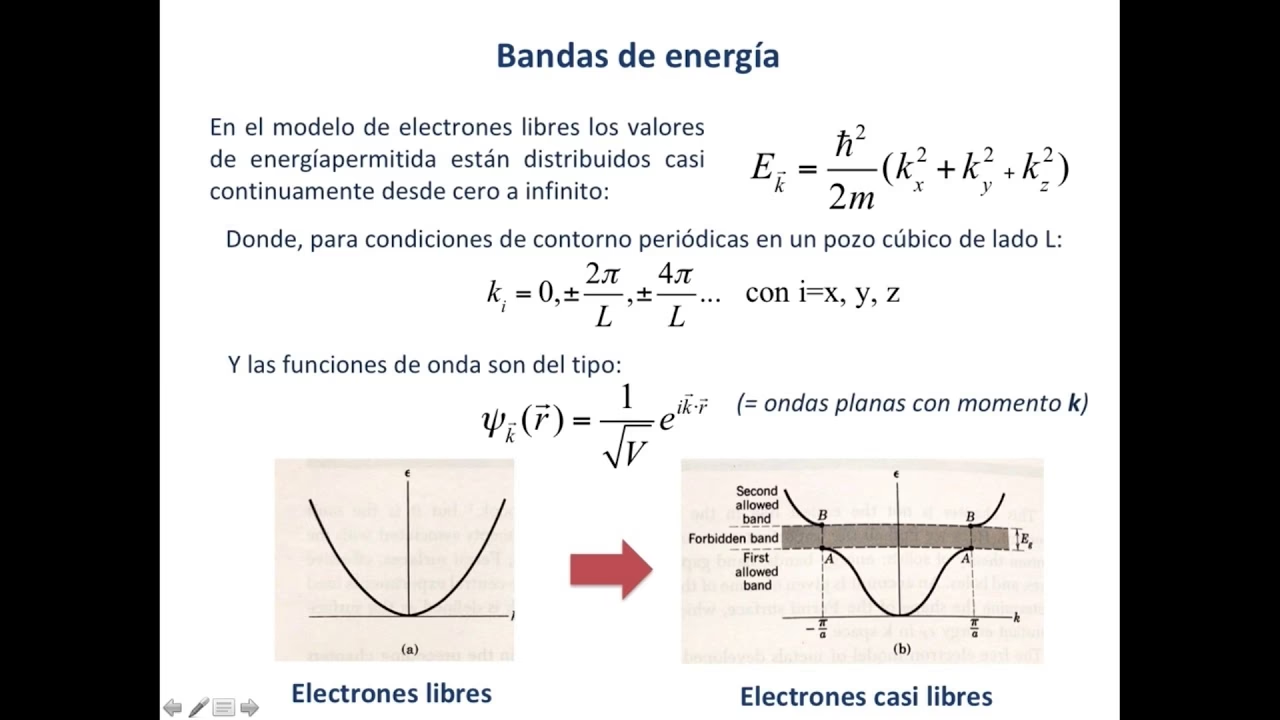
Cuando los átomos se agrupan para formar un material sólido, como un metal o un cristal de silicio, sus niveles de energía individuales interactúan y se superponen. En lugar de tener niveles de energía discretos y nítidos, se forman amplias bandas de energía. Dentro de estas bandas, los electrones pueden tener cualquier valor de energía. Las dos bandas más importantes son:
La diferencia de energía entre estas dos bandas se llama “bandgap” o brecha energética. Esta brecha determina las propiedades eléctricas del material. En los semiconductores, como el silicio utilizado en los paneles fotovoltaicos, esta brecha es lo suficientemente pequeña como para que los fotones de la luz solar puedan proporcionar la energía necesaria para que los electrones salten de la banda de valencia a la de conducción, generando así una corriente eléctrica. Este es el corazón del efecto fotovoltaico.
Según la física clásica, un electrón en órbita debería irradiar energía y caer en espiral hacia el núcleo. Sin embargo, la mecánica cuántica establece que los electrones existen en estados estacionarios (orbitales) con niveles de energía mínimos. No pueden perder más energía una vez que alcanzan su nivel fundamental (n=1), por lo que no pueden colapsar sobre el núcleo.
Es la descripción detallada de cómo se distribuyen todos los electrones de un átomo entre los diferentes niveles y subniveles de energía. Se escribe siguiendo reglas específicas, como el Principio de Aufbau, que dicta que los electrones llenan primero los orbitales de menor energía.
No. Aunque los 7 niveles de energía existen teóricamente para cualquier átomo, en su estado fundamental (no excitado), los átomos solo llenan los niveles necesarios para acomodar su número total de electrones. Por ejemplo, el sodio (11 electrones) solo llena los niveles 1, 2 y tiene un electrón en el nivel 3.
La relación es fundamental. La tecnología fotovoltaica se basa en el material semiconductor del panel (generalmente silicio). La energía de un fotón de luz solar golpea un electrón en la banda de valencia del silicio. Si esta energía es suficiente para superar la brecha energética (el “bandgap”), el electrón es “excitado” y salta a la banda de conducción. Una vez en la banda de conducción, este electrón es libre de moverse, y un campo eléctrico incorporado en la célula solar lo dirige para crear una corriente eléctrica, que es la electricidad que utilizamos.

Descubre qué es una granja solar, también llamada huerto o parque fotovoltaico. Te explicamos cómo...

¿Alguna vez te has preguntado cómo esa pequeña tira en tu calculadora la hace funcionar...

Salta enfrenta serios desafíos ambientales como la deforestación y la contaminación. Descubre cómo la energía...

Descubre cuánto gana un ingeniero en energías renovables en Argentina. Analizamos los factores clave: experiencia,...