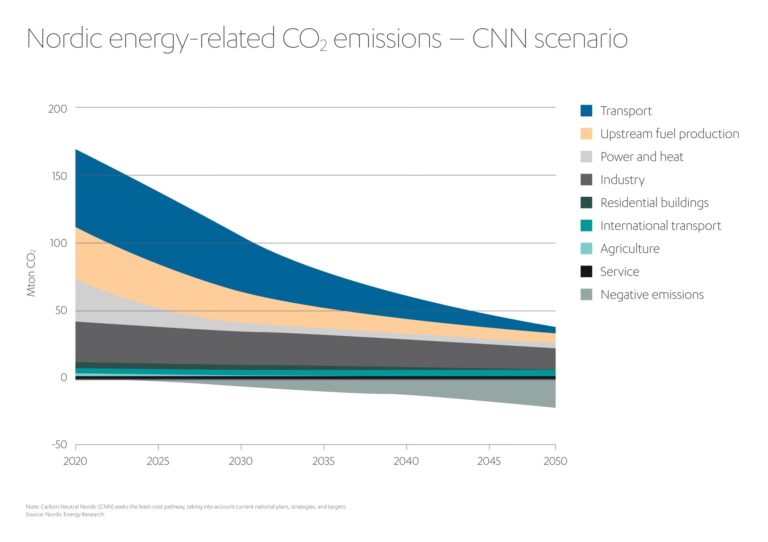
Países Nórdicos: Líderes en Energía Renovable
Descubre cómo los países nórdicos se han convertido en la región más sostenible del mundo....
Para comprender verdaderamente cómo un panel solar en nuestro tejado puede encender una bombilla, debemos viajar al corazón de la materia, a un mundo invisible donde las reglas de la física clásica se desvanecen. Hablamos del mundo del átomo y, más específicamente, del comportamiento de sus partículas más dinámicas: los electrones. La forma en que estos electrones se organizan y mueven es la clave no solo de toda la química, sino también de la tecnología fotovoltaica que aprovecha la energía del sol. No se trata de magia, sino de una danza cuántica precisa que ocurre en niveles de energía definidos.
Imaginemos el átomo como un sistema solar en miniatura. En el centro se encuentra el núcleo, pesado y con carga positiva, y orbitando a su alrededor, como planetas, están los electrones, con carga negativa. Este fue el modelo propuesto por Niels Bohr a principios del siglo XX, un paso gigantesco en nuestra comprensión. Bohr sugirió que los electrones no podían orbitar a cualquier distancia del núcleo, sino que estaban confinados a órbitas específicas o “niveles de energía”.
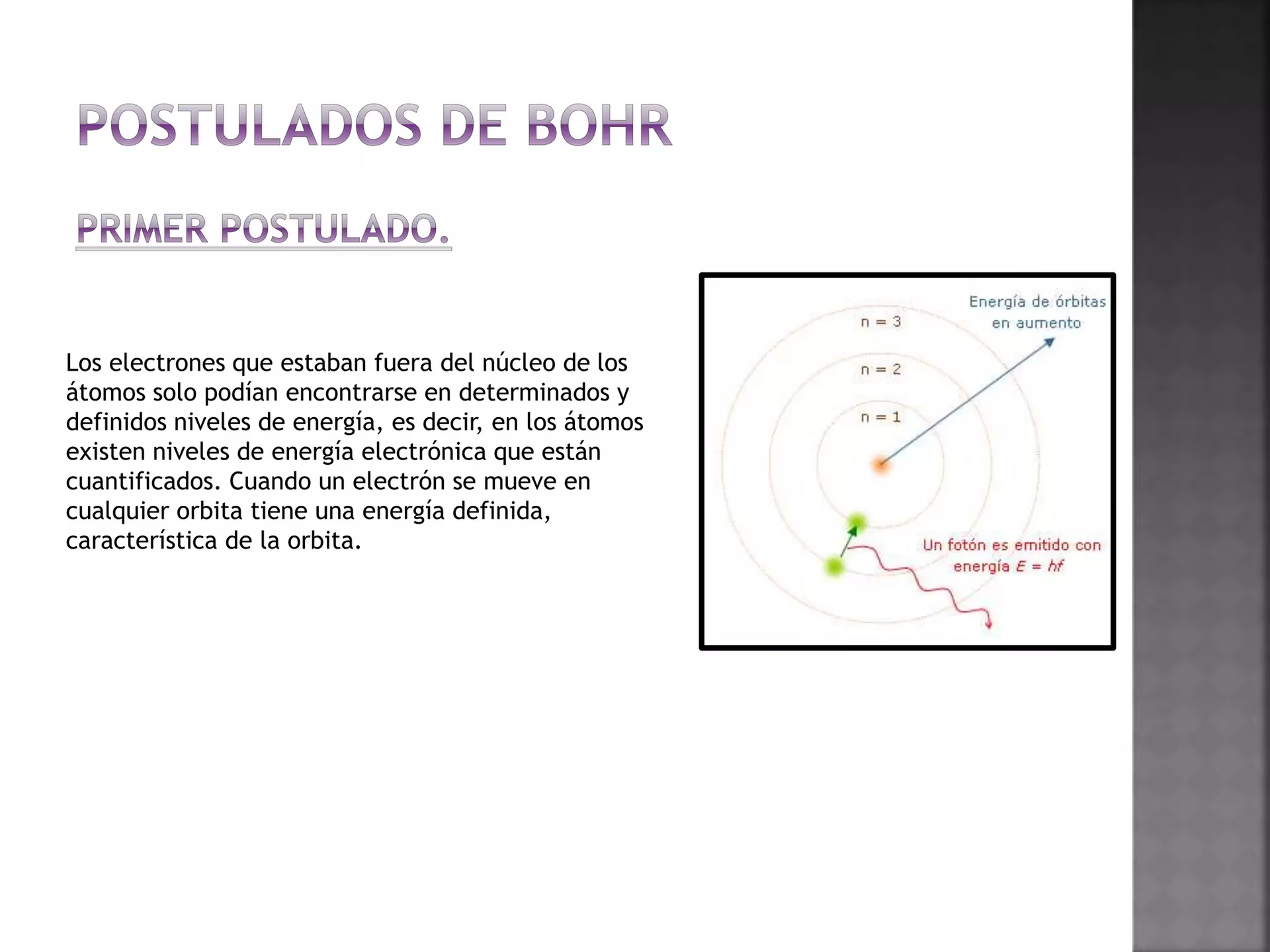
Podemos pensar en estos niveles como los peldaños de una escalera. Un electrón puede estar en el primer peldaño o en el segundo, pero nunca puede flotar en el espacio intermedio. Cada peldaño representa una cantidad fija y discreta de energía. Cuanto más alejado está un electrón del núcleo (cuanto más alto es el peldaño), mayor es su nivel de energía. Este concepto, aunque posteriormente refinado por la mecánica cuántica, sigue siendo la base para entender cómo los átomos interactúan con la luz y la energía.
Aunque el modelo de Bohr fue revolucionario, tenía sus limitaciones. Por ejemplo, no podía explicar por qué algunas líneas en los espectros de luz eran más brillantes que otras y violaba el Principio de Incertidumbre, que establece que no podemos conocer simultáneamente la posición y el momento exactos de un electrón. Hoy sabemos que los electrones no siguen órbitas planetarias perfectas, sino que existen en “orbitales”, que son regiones de probabilidad donde es más probable encontrarlos. Sin embargo, la idea fundamental de niveles de energía cuantificados perdura.
El verdadero motor de la interacción entre la materia y la energía reside en la capacidad de los electrones para “saltar” entre estos niveles. Un electrón en un nivel de energía bajo (más cercano al núcleo) puede absorber una cantidad exacta de energía y saltar a un nivel superior, más alejado. Esta energía puede provenir de diversas fuentes, como el calor o, crucialmente para nosotros, la luz. Este estado se conoce como “estado excitado”.
Sin embargo, este estado es inestable. El electrón tiende a regresar a su nivel de energía original, más bajo y estable. Al hacerlo, debe liberar la energía extra que había absorbido. Esta energía se emite a menudo en forma de un fotón, una partícula de luz. El color (o la longitud de onda) de esa luz depende exactamente de cuánta energía se libera, es decir, de la diferencia de energía entre los dos niveles.

Un ejemplo espectacular de este fenómeno son los fuegos artificiales. Cuando los compuestos químicos en un fuego artificial explotan, el calor proporciona la energía para que los electrones de diferentes átomos salten a niveles más altos. Inmediatamente, caen de nuevo a sus niveles originales, emitiendo luz de colores característicos: el estroncio emite rojo, el bario emite verde, el cobre emite azul. Cada color corresponde a un salto energético específico de los electrones de ese elemento en particular.
Los átomos no distribuyen sus electrones al azar. Siguen una regla fundamental conocida como el principio de mínima energía o Principio de Aufbau. Esto significa que los electrones siempre ocuparán primero los niveles y orbitales de menor energía disponibles, los más cercanos al núcleo, antes de empezar a llenar los niveles superiores.
Cada nivel de energía se subdivide en uno o más orbitales, cada uno con una forma particular (esférica, de lóbulo, etc.). Independientemente de su forma, cada orbital puede albergar un máximo de dos electrones. Veamos cómo se estructura:
El orden de llenado no siempre es lineal. Por ejemplo, el orbital 4s tiene ligeramente menos energía que los orbitales 3d, por lo que se llena primero. Este ordenamiento preciso es lo que da a cada elemento de la tabla periódica su configuración electrónica única y, por tanto, sus propiedades distintivas.
De todos los electrones de un átomo, los más importantes para la química y la generación de energía son los que se encuentran en el nivel de energía más externo. Estos se conocen como electrones de valencia. Su comportamiento determina si un átomo es estable, si reaccionará con otros átomos y cómo lo hará.

Un átomo alcanza su máxima estabilidad cuando su capa de valencia está completamente llena. Los gases nobles, como el Helio o el Neón, son ejemplos perfectos. El Neón tiene 10 electrones: 2 en el primer nivel y 8 en el segundo. Como el segundo nivel está lleno con 8 electrones, el Neón es extremadamente estable y no reactivo.
Por otro lado, un átomo como el Litio, con solo un electrón de valencia, tiende a perderlo para quedarse con su capa interna llena y estable. Un átomo como el Flúor, con siete electrones de valencia, busca desesperadamente ganar un electrón para completar su capa de ocho. Esta tendencia a ganar, perder o compartir electrones de valencia es la base de todos los enlaces químicos.
Ahora podemos entender el secreto detrás del efecto fotovoltaico. Los paneles solares están hechos principalmente de silicio, un material semiconductor. Un átomo de silicio tiene cuatro electrones de valencia. En un cristal de silicio, estos átomos se enlazan compartiendo sus electrones de valencia, creando una estructura estable donde los electrones están firmemente sujetos en lo que se conoce como la “banda de valencia”.
Cuando la luz del sol (que es un flujo de fotones) incide sobre el panel solar, ocurre lo siguiente:
Así, cada fotón que golpea el panel y excita un electrón está repitiendo, a una escala masiva, el mismo principio de salto entre niveles de energía que hemos descrito. La energía de la luz solar se convierte directamente en energía eléctrica gracias a las propiedades cuánticas de los electrones en el material semiconductor.
| Característica | Modelo de Bohr (Clásico-Cuántico) | Modelo Mecánico-Cuántico (Moderno) |
|---|---|---|
| Naturaleza del electrón | Partícula en una órbita definida. | Comportamiento dual onda-partícula. |
| Ubicación | Órbitas circulares fijas y predecibles. | Orbitales: regiones de alta probabilidad. |
| Principio de Incertidumbre | Lo viola (posición y momento definidos). | Lo respeta (no se puede conocer ambos con precisión). |
| Utilidad | Excelente modelo conceptual para introducir los niveles de energía. | Descripción precisa y matemática del comportamiento atómico. |

Descubre cómo los países nórdicos se han convertido en la región más sostenible del mundo....

Descubre cómo una empresa en Kerala, India, lanzó el primer autobús local con aire acondicionado...

Descubre si instalar paneles solares en Alabama es la decisión correcta para ti. Analizamos costos,...

Descubre qué es un parque solar o fotovoltaico, cómo funciona y para qué sirve. Conoce...