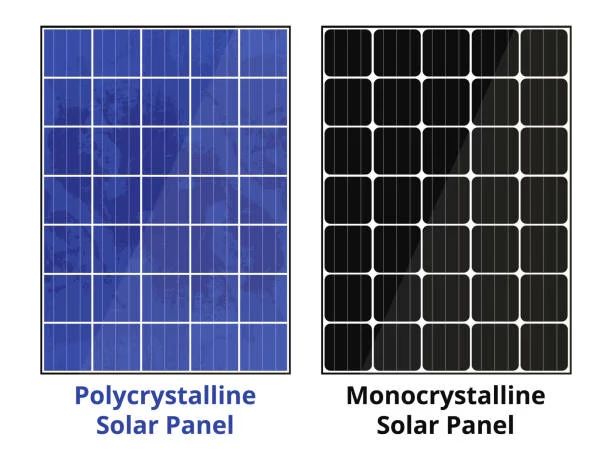
Panel Monocristalino vs Policristalino: Guía 2024
¿Pensando en instalar paneles solares? Descubre las diferencias clave entre paneles monocristalinos y policristalinos. Eficiencia,...
En el vasto universo de la física y la energía, existen principios fundamentales que gobiernan cada proceso, desde el parpadeo de una estrella hasta el funcionamiento de un termotanque solar en nuestro techo. Uno de los pilares más importantes es la Primera Ley de la Termodinámica. A menudo resumida en la célebre frase “la energía no se crea ni se destruye, solo se transforma”, esta ley es, en esencia, una declaración de la conservación de la energía. Es el balance contable del universo, asegurando que cada julio de energía sea rastreado, sin importar cómo cambie de forma. En este artículo, desglosaremos esta ley crucial para entender cómo interactúan el calor, el trabajo y la energía interna, y por qué es tan relevante para las tecnologías de energía renovable que nos apasionan.

La Primera Ley de la Termodinámica establece una relación precisa entre tres cantidades clave: la energía interna de un sistema, el calor que se le transfiere y el trabajo que realiza. Para comprenderla, primero debemos definir a nuestros protagonistas:
Con estos conceptos, la ley se expresa matemáticamente de una forma muy elegante:
ΔU = Q – W
Esto se lee así: el cambio en la energía interna (ΔU) de un sistema es igual al calor (Q) añadido al sistema, menos el trabajo (W) realizado por el sistema. Es una fórmula simple pero increíblemente poderosa.
Para aplicar correctamente la fórmula, es vital entender la convención de signos, que nos dice si la energía está entrando o saliendo del sistema. Es como llevar la contabilidad de un negocio: los ingresos son positivos y los gastos son negativos.
| Proceso | Convención de Signo | Explicación |
|---|---|---|
| Calor añadido al sistema | Q > 0 (Positivo) | El sistema gana energía. Ej: El sol calentando un panel solar. |
| Calor extraído del sistema | Q < 0 (Negativo) | El sistema pierde energía. Ej: Un objeto caliente enfriándose. |
| Trabajo realizado por el sistema | W > 0 (Positivo) | El sistema gasta energía para actuar sobre su entorno. Ej: Un gas expandiéndose. |
| Trabajo realizado sobre el sistema | W < 0 (Negativo) | El entorno le da energía al sistema. Ej: Comprimiendo un gas. |
Una de las ideas más profundas asociadas a esta ley es que la energía interna es una “función de estado”. ¿Qué significa esto? Imagina que quieres escalar una montaña. Tu punto de partida es el Estado A (la base) y tu destino es el Estado B (la cima). La diferencia de altitud entre A y B es siempre la misma, sin importar el camino que tomes. Puedes elegir una ruta corta y empinada o una larga y sinuosa; la ganancia de altitud final será idéntica.
La energía interna (U) es como esa altitud. El cambio en la energía interna (ΔU) entre un estado inicial y uno final solo depende de esos estados, no del proceso o “camino” termodinámico que los conectó. En cambio, el calor (Q) y el trabajo (W) son como el esfuerzo y el tiempo que te tomó escalar: dependen totalmente del camino elegido. Aunque Q y W pueden variar mucho entre diferentes procesos, su diferencia (Q – W) siempre será la misma para los mismos puntos de inicio y fin, porque esa diferencia es, por definición, ΔU.
La Primera Ley no es solo teoría; es la base para diseñar y entender casi cualquier sistema energético.
La Primera Ley nos permite analizar diferentes tipos de procesos ideales que son fundamentales en la ingeniería y la física.
| Tipo de Proceso | Condición Constante | Consecuencia en la 1ª Ley | Ejemplo Práctico |
|---|---|---|---|
| Isotérmico | Temperatura (ΔT = 0) | Para un gas ideal, ΔU = 0, por lo que Q = W. | Una expansión muy lenta de un gas en contacto con un gran depósito de calor. |
| Isocórico | Volumen (ΔV = 0) | No hay cambio de volumen, por lo que W = 0. La ley se simplifica a ΔU = Q. | Calentar gas en un recipiente rígido y sellado. |
| Isobárico | Presión (P = cte.) | La fórmula completa se aplica: ΔU = Q – W, donde W = PΔV. | Hervir agua en una olla abierta (la presión es la atmosférica). |
| Adiabático | Sin intercambio de calor | Q = 0, por lo que la ley se convierte en ΔU = -W. | Un gas que se expande rápidamente desde una lata de aire comprimido (se enfría porque el trabajo lo hace a costa de su propia energía interna). |
R: No, todo lo contrario. Implica que la cantidad total de energía en un sistema aislado (como el universo) es finita y constante. No podemos “crear” nueva energía para resolver nuestras necesidades; solo podemos transformarla de las fuentes que ya existen, como el sol, el viento o los combustibles fósiles.
R: La Primera Ley de la Termodinámica prohíbe las llamadas “máquinas de movimiento perpetuo de primer tipo”. Estas serían máquinas que producen más energía (en forma de trabajo) de la que consumen, violando directamente el principio de conservación de la energía. Simplemente, no puedes obtener más energía de la que pones.
R: Esta es una excelente pregunta que nos lleva a la Segunda Ley de la Termodinámica. Aunque la cantidad total de energía se conserva, su *calidad* o *utilidad* no. Cada vez que transformamos energía, una parte se degrada inevitablemente a una forma menos útil, generalmente calor a baja temperatura. “Ahorrar energía” en realidad significa usar la energía de alta calidad de manera más eficiente para evitar su degradación innecesaria.
R: Tu cuerpo es un sistema termodinámico. La comida que ingieres es el aporte de energía química (similar a Q). Realizas trabajo (W) al moverte, levantar objetos o incluso al hacer que tu corazón bombee. También liberas calor al ambiente. El balance entre la energía que consumes y la que gastas (como trabajo y calor) determina si tu energía interna aumenta (ganas peso) o disminuye (pierdes peso).
La Primera Ley de la Termodinámica es mucho más que una ecuación en un libro de texto. Es el principio fundamental que confirma que no hay “almuerzo gratis” en el universo energético. Cada dispositivo que usamos, desde una simple estufa hasta un complejo climatizador solar de piscinas, opera bajo esta regla inmutable. Entenderla nos permite no solo apreciar la elegancia de la naturaleza, sino también diseñar tecnologías más eficientes y sostenibles que aprovechen las transformaciones energéticas de la manera más inteligente posible, respetando el balance fundamental del cosmos.

¿Pensando en instalar paneles solares? Descubre las diferencias clave entre paneles monocristalinos y policristalinos. Eficiencia,...

¿Quieres saber cuánta energía produce realmente un panel solar? Descubre qué es el rendimiento, cómo...

Descubre cómo obtener paneles solares sin costo inicial en Illinois con el programa ILSFA. ¡Aprovecha...

Descubre qué es la Diplomatura en Energía y cómo te prepara para liderar la transición...